Personalized CT imaging with SOMATOM Force
Thomas Henzler, M.D.(CT Institute of Clinical Radiology and Nuclear Medicine, University Medical Center Mannheim)
<Session V Special Lecture>
2014-11-25

マンハイム大学病院では2013年9月から,新開発のX線管「VECTRON」など,さまざまな最先端技術を搭載した新型Dual Source CT「SOMATOM Force」の世界第1号機が稼働を開始した。本講演では,臨床現場に変化をもたらす新システムであるSOMATOM Forceについて,(1) 造影剤量の低減,(2) 被ばく低減,(3) CTによる機能イメージング,(4) 超高速撮影による鎮静不要CT検査を中心に報告する。
造影剤量低減
1.Low kV撮影による造影剤量の低減
SOMATOM Forceにて,経カテーテル大動脈弁置換術(TAVI)の治療計画を実施する場合,患者の多くは腎機能不全であるため,造影剤腎症を避けるには造影剤量の低減を図らなければならない。
SOMATOM Forceでは,管電圧選択を70kVにすることでコントラストノイズ比(CNR)を改善する。寝台移動速度を上げるとともに新開発の検出器とVECTORONにより高速撮影が可能となり,わずか1秒で全身のスキャンができる。それにより造影剤量の低減が可能であり,実際に,150mL必要であった体格の大きなドイツ人においても40mLに低減可能であった。ただし,撮影速度がボーラス速度よりも速くなる可能性があるため,造影剤投与タイミングがきわめて重要である。
Case1では,70kVのLow kVイメージングにより造影剤量をさらに低減できた。20mLの造影剤を生理食塩水で50%希釈して使用したが,頸動脈および総腸骨動脈内の十分な造影効果が得られている(図1)。
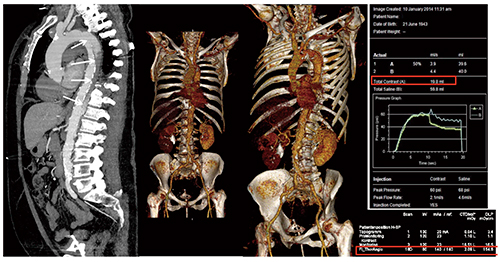
図1 Case1:Low kVイメージングによる造影剤量の低減
(Whole-Body CT,70kV,造影剤量20mL)
この70kVでのLow kVイメージングは,ルーチンで使用可能である。Case2は,当院にて大動脈の人工血管および塞栓の評価に使用している4Dイメージングプロトコルで撮影した画像である(図2)。軸方向で80cmまでカバーできるが,造影剤量はわずか12mLであり,テストボーラスに使用する量をわずかに上回る程度であるため,ボーラストラッキングもテストボーラスも行っていない。最終的には70kVで12回のシャトルスキャンを行うが,ドイツの連邦放射線防護局が定める基準線量値の範囲内である。これは,CTにおける4Dイメージングの先端を行くものと言え,今後の診断体系も変わると言える。
一方,70kVにより生じる平均光子エネルギーに着目すると,80kVや120kVと比較してk-edgeの増大が見られる。これが,造影剤を希釈してもこれほど高い血管のX線減弱が得られる理由である。
では,なぜこれまでLow kVイメージングがルーチンで行われなかったのかというと,低管電圧で十分な光子出力が得られるX線管がなかったためである。SOMATOM Forceでは,2つのVECTRON Tubeが搭載されており,Low kVで高い管電流が得られる。そのため,70kVでも1300mAという高出力が可能であり,当院ではBMI:33までの患者は70kVで撮影しているが,十分な画質が得られている。
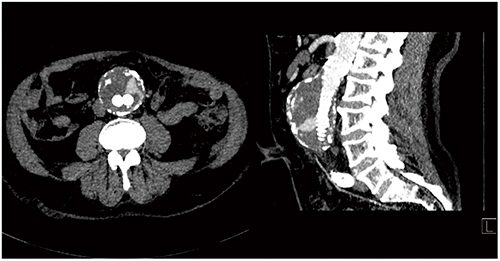
図2 Case2:72歳,大動脈ステントグラフト挿入術後のエンドリーク
(70kV,造影剤量12mL)
2.Dual Energy CT(DECT)における造影剤量の低減
最適な造影効果を得るためのもう1つの技術として,DECTによるmix imagingやmonoenergetic imagingがある。これは,高エネルギーと低エネルギーの2種類の画像から任意の管電圧や実効エネルギーの画像を得る技術である。High keV画像を再構成することで金属アーチファクトが低減できるほか,あらゆるCTスキャンで血管のX線減弱を増大させることができる。
SOMATOM Forceでは,新しいmonoenergetic imaging技術として,“Monoenergetic Plus”が登載されている。これは優れたアルゴリズムであり,Low kVのデータセットから血管強調された低空間周波数画像とOptimal kVのデータセットから高空間周波数画像を取得し,1つのデータセットとして算出する。これにより,低いノイズレベルで血管強調されたmonoenergetic imageが得られ,40keVの画像を再構成することができる。現在,われわれはクレアチニン値の高いハイリスク患者に使用し,40keVの画像にて評価を行っている。これは造影剤を低減する第2のアプローチである。
Case3は,77歳,血中クレアチニン値の高いTAVI適応症例である。本症例における使用造影剤量は,大動脈全体で15mLであり,それを50%に希釈しているため120kVpでは画質が低下するが,Monoenergetic Plusの40keV画像では,TAVIの治療計画を立てる上で十分な画質が得られている(図3)。
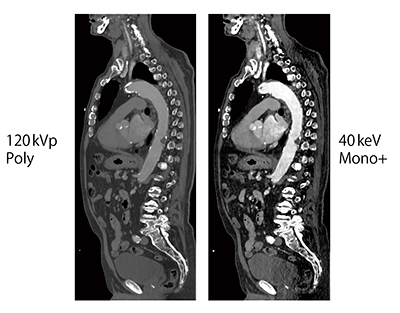
図3 Case3:77歳,血中クレアチニン値の高いTAVI適応症例のMonoenergetic Plus画像(造影剤量15mL)
被ばく線量の低減
1.循環器領域
図4は,異なるサイズのファントムにおける放射線量と管電圧の関係であるが,管電圧を70kVまで下げると,きわめて低線量のCTDIvolを示した。これは,今後さらに期待されるサブミリシーベルト心臓CTにきわめて有利である。SOMATOM Forceでは,心拍数が75bpmの高心拍の患者においてもTurbo Flash Spiralにより1心拍撮影が可能である。加えて,70kVできわめて高い造影効果が得られるため,造影剤量をさらに低減できる可能性がある。
心臓CTにおいても,選択可能なあらゆる技術において最適な線量を用いることが重要である(Right Dose Imaging)(図5)。また,SOMATOM Forceでは,第三世代の逐次近似画像再構成法である“ADMIRE(Advanced Modeled Iterative Reconstruction)”により,さらなる画質の向上が可能である。Case4は,ステント内腔評価のため受診した症例である。分解能の向上に加え,ステント内のブルーミングアーチファクトが低減されており,ステント内狭窄を適切に診断できる(図6)。また,非石灰化プラークも,きわめて良好に描出されている。
心臓CTを救急対応を含め24時間実施することは大きな課題であるが,当院には経験の浅いレジデントのための夜間用プロトコルがある。これは,管電流を大幅に低減しない70kVのプロトコルであり,2.3mSv程度での撮影が可能である。翌日,担当医が画像を参照して心機能の評価を行えるため,左室(LV)機能を見ることで,例えば大動脈二尖弁やたこつぼ型心筋症が確認されることもあるなど,臨床上多くの追加情報が得られている。
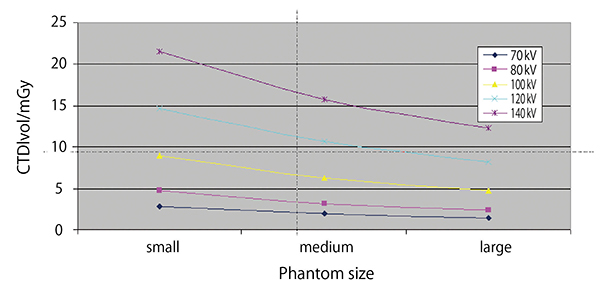
図4 異なるサイズのファントムにおける放射線量と管電圧の関係
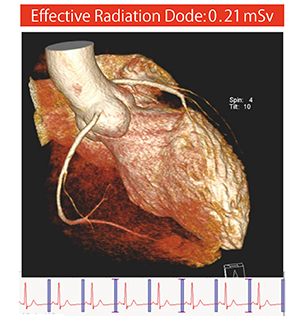
図5 Right Dose Imaging:70kV Retrospective ECG-Gating
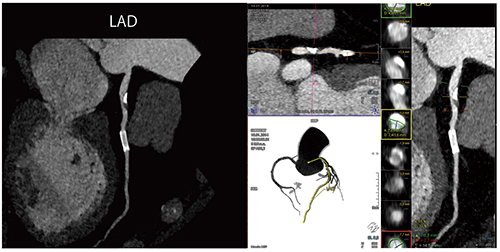
図6 Case4:69歳,ステント内腔狭窄疑い(造影剤量40mL,DLP 250mGy・cm)
2.頭部領域
SOMATOM Forceの空間分解能について述べる。側頭骨は高分解能画像が求められる部位である。小児患者は耳出血のため側頭骨の精査目的のCT検査を受けることが多いが,その際,水晶体の被ばくが問題となる。しかし,SOMATOM Forceの焦点スポットは0.4mm×0.5mmで一般的なCTの小焦点の約半分であり,また,0.4mmスライス厚画像を取得可能なため超高分解能グリッドを用いる必要がなく,被ばくの懸念も低くなる(図7)。
脳梗塞疑いの頭部ルーチンを対象にSOMATOM Forceと別のCTとを比較したスタディでは,SOMATOM Forceの方が被ばく線量が有意に低く,ノイズのない画像が得られている。これは特に,頭蓋と白質の区別を著明に向上させるために重要である。
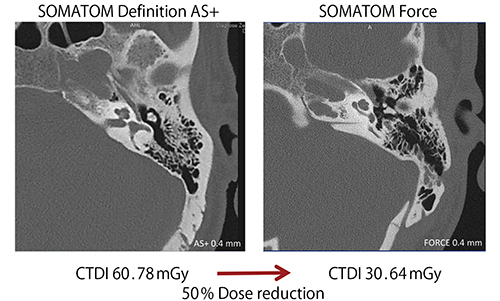
図7 側頭骨のCT画像:SOMATOM Definition AS+(zUHRフィルタあり)と
SOMATOM Force(zUHRフィルタなし)の比較
3.肺野領域
SOMATOM Forceのもう1つの重要な特長は,超低被ばくの胸部CTイメージングが可能なことである。これは,「X線スペクトル変調イメージング」,あるいは「Tin Filterイメージング」とも呼ばれている。
X線管にSPSⅡ(Selective Photon Shield Ⅱ):Tin Filterが搭載されており,X線スペクトルを変調している。これにより,100kVで発生するX線スペクトルの低エネルギースペクトルを低減し,高エネルギースペクトル優位なX線が得られる。その結果,非常に高画質かつ超低被ばくでの胸部検査が可能となる。これによりさまざまな可能性が考えられるが,何より0.1mSvできわめて高精度な画像が得られることが重要である。今後,冠動脈石灰化の評価をはじめ,本プロトコルを用いた多くの研究が期待される。
さらに,われわれは腫瘍科の患者に対するルーチン検査に本プロトコルを応用し,air trappingや閉塞性細気管支炎の鑑別に役立てている(図8)。非定型肺炎と移植片対宿主拒絶反応との鑑別の精度向上にも有用である。
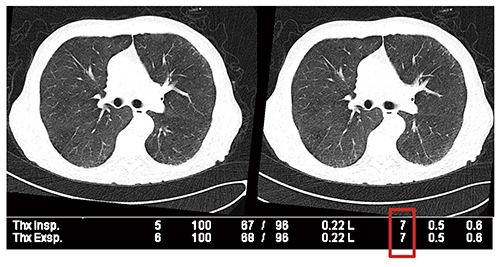
図8 超低線量胸部CTによる閉塞性細気管支炎の鑑別診断
(100kV with tin filter →0.098mSv/scan)
CTによる機能イメージング
1.4D Perfusion CT
SOMATOM Forceによる機能イメージングの手法には,シャトルモードとスパイラル撮影,およびDual Energyモードがあり,いずれの技術も腫瘍および心血管イメージングに適用可能である。なかでもDynamic 4D Shuttle Mode Perfusion CTは,固形腫瘍,膵腫瘍の診断に有用である。70kVで優れた血管造影像が得られ,腫瘍サイズのほか,血流量,血液量など多くのことがわかるため,定位放射線治療の治療計画にも有用である。
Case5は,Dynamic 4D Shuttle Mode Perfusion CTが腫瘍検出に有用であった神経内分泌腫瘍の転移例であるが,単純CTおよびMRIではいずれも陰性だった。Dynamic 4D Shuttle Mode Perfusion CTでは,シネイメージを確認すると,撮影開始の3.5秒後のわずかの時間に腫瘍濃染が描出されていた。このように,本手法は治療応答性の評価はもとより,腫瘍検出や肝細胞がんの診断にも有用である(図9)。
また,治療効果を評価するツールとしてもDynamic 4D Shuttle Mode Perfusion CTは有用である。Case6は血管筋脂肪腫である。術前の4D-CTで最適な時相を選択することで,静脈系と動脈系を正確に区別することができる(図10)。
従来のゴールドスタンダードであるPerfusion MRIでは, 1.5Tから3Tになると多くの違いが出てくるが,Perfusion CTによる灌流分析は非常に安定している。このことは,腫瘍の経過観察において重要であり,最近では,4D撮影を経時的に複数回行う5D-CTも実施している。
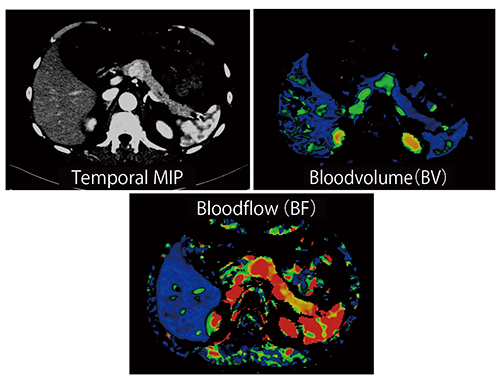
図9 Case5:神経内分泌腫瘍の転移例のDynamic 4D Shuttle Mode Perfusion画像(70kV)
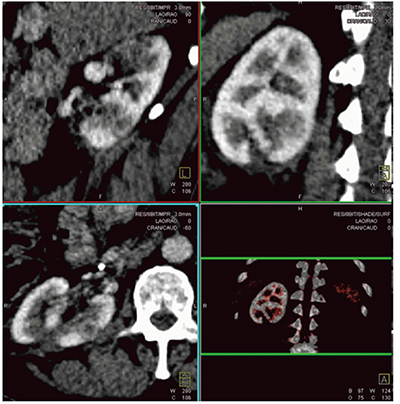
図10 Case6:血管筋脂肪腫の術前4D-CT画像
2.Dual Energy CT(DECT)
DECTにおいて最も重要なことは,2つのエネルギーのX線スペクトルが正確に区別ができることであるが,SOMATOM Forceでは,さまざまな管電圧の組み合わせによるDECTが可能となった。
新たな組み合わせとして,150kVにTin Filterを用いて100/150kVで実施することができるほか,90kV,80kVとの組み合わせも可能である。
DECTが最も威力を発揮するのは,virtual non-contrast imagingであると考えている。図11は胃がん患者のvirtual non-contrast画像であり,従来のvirtual non-contrast画像では,特に体格の大きな患者などは十分な画質が得られない場合があったが,これは本物の非造影画像のように見える。その要因の1つとして,SOMATOM Forceのエナジーセパレーション(X線分離能力)の高さが挙げられる。
Case7は,消化管間質腫瘍(GIST)の転移であり,サイズ評価に基づけば進行性の症例である(図12)。ヨウ素取り込みに着目すると,最初のスキャン(図12左)では約33%であったが,フォロースキャン(図12右)では約13%に低減しており,粘液型の進行がんと診断できた。本症例は安定しており,治療への応答性があるため,治療変更の適応とはならない。このように,イメージングが治療決定に影響を及ぼしうることがわかる。
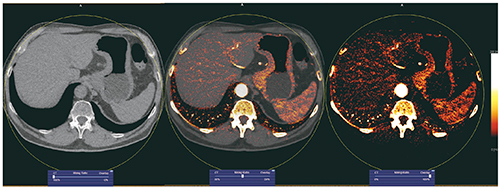
図11 胃がん患者のvirtual non-contrast画像(90/150kV)
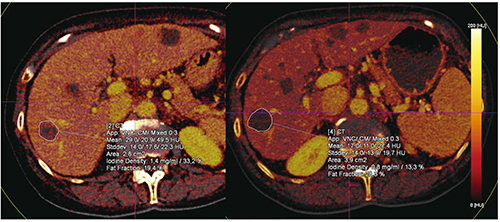
図12 Case7:GIST症例のヨウ素増強画像による腫瘍鑑別評価
3.心血管イメージングにおける4D Perfusion CT/DECTの有用性
心血管イメージングにおいて4D Perfusion CTは,SOMATOM Forceと4D-CTを撮影可能な他の装置とを差別化する大きな違いの1つであると考えている。
Case8は左総腸骨動脈の閉塞症例であるが,大規模なバイパス術の適応となるのか,総腸骨動脈のみの血管再建術の適応となるのかを,4D CTAにて容易に判断できる(図13)。
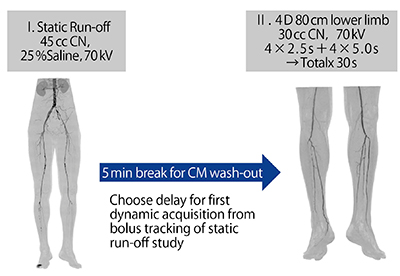
図13 Case8:左総腸骨動脈完全閉塞症例
4D CTAはステントの評価にも有用である。Case9はステント内狭窄疑いの症例である。シネモードで時系列画像を詳しく見ると,側副動脈およびステントの血行動態的に著明な狭窄がないことが明確にわかる(図14)。
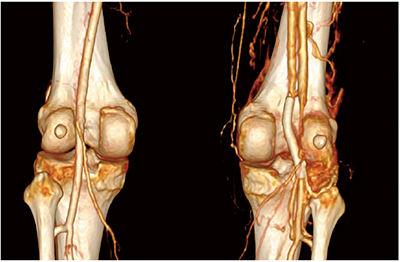
図14 Case9:ステント内狭窄疑い症例の4D CTA画像
もうひとつ強調したいのは,CT静脈造影の画質の高さである。70kVでスキャン可能なため,非常に満足できる画像が得られている。
さらに魅力的なのは,瘻孔のイメージングである。Case10は,瘻孔の狭窄症例である(図15)。このように広範囲をすべてカバーする画像をIVR医や心臓血管外科医に提供することにより,適切な治療計画を行うことができる。経時的に見ると,時間の経過とともに血栓による静脈系の充満を見ることができる。これは完全に新しい適応であり,CTにおける新たなアプローチである。
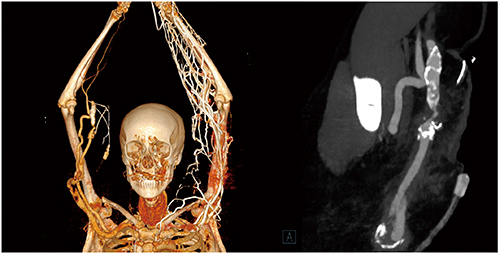
図15 Case10:瘻孔狭窄症例の4D CTA画像
心筋血流イメージングにおいては現在,冠血流予備量比(FFR)の測定がゴールドスタンダードであるが,実際にはDECT,Perfusion,FFRのどれが最も優れているかは,いまのところ不明である。しかし,SOMATOM ForceにてStep and Shoot ModeでDECT画像を取得できるようになったことは,良いニュースである。以前はスパイラルモードに限定されていたが,SOMATOM Forceでは2ステップでDual Energy 撮影ができるため,従来と比較して放射線量を低減できる(図16)。また,DECTにおける遅延造影CTは大変興味深い。なぜなら,Low kVデータセットを観察することにより,遅延造影CT画像のヨウ素増強をより強調できる可能性があるためである。
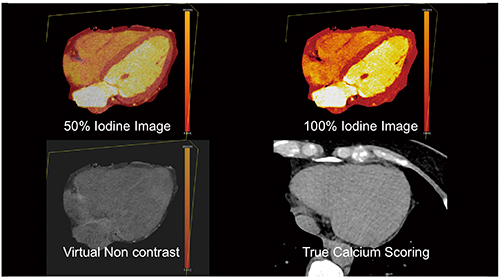
図16 Step and Shoot Modeを用いたDECTによる心血管イメージ
さらに,SOMATOM Forceでは心臓全体をカバーした心筋Dynamic Perfusionが簡便に可能なほか,MRIよりも優れている点として,特に冠動脈三枝病変の診断に重要な定量評価が可能なアプリケーションを有していることが挙げられる(図17)。
また,脳卒中のイメージングでも同じことが可能である。脳だけでなく,頸動脈のPerfusion撮影と組み合わせることが可能で,診断,評価にとても役立つ。
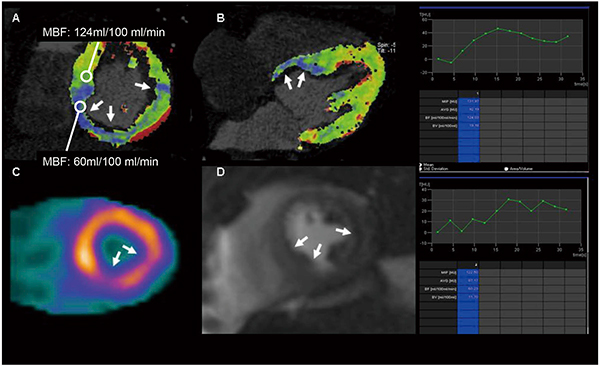
図17 心筋CT Perfusionの定量評価
Sedation Free CT(鎮静不要CT)
小児の撮影法は現在二通りしかなく,鎮静するか,体動・呼吸下での撮影である。しかし,SOMATOM Forceでは,「Sedation Free CT」(鎮静不要CT)が可能である。
Case11は生後32日の新生児で,検査中に泣いていたが,わずか0.1秒の撮影のため体動アーチファクトは見られない。加えて,DLP 1.3mGy・cmと非常に低い被ばく線量を達成しつつ,画質はきわめて良好である(図18)。
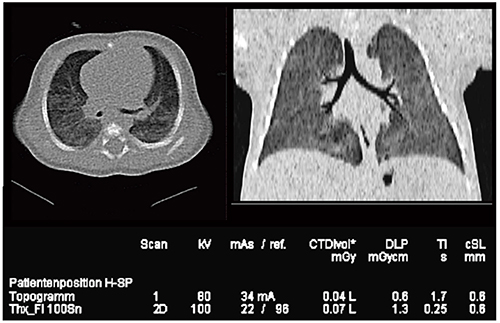
図18 Case11:70kVのSedation Free CT(生後32日,新生児)
Case12は他院で鎮静を行ってCT撮影をした小児の例であるが,鎮静をしても体動アーチファクトが見られるのに対し(図19 a),数か月後にSOMATOM Forceにて行った鎮静なしのハイピッチ撮影では体動アーチファクトは見られず(図19 b),DLPも約88 mGy・cmから約12 mGy・cmに低減している。
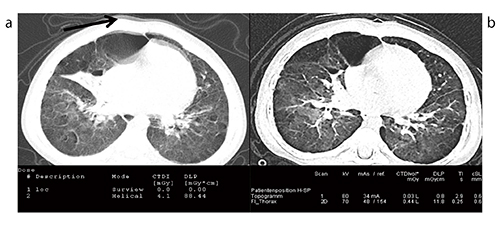
図19 Case12:低線量でのSedation Free CT〔従来CT(a)との比較〕
(70kV,DLP 11.8mGy・cm)
まとめ
SOMATOM Forceは,今までのCTの診断アプローチを大きく変えるポテンシャルを秘めている。また,CT検査でのさまざまなハードルが下がった低侵襲な検査が可能と思われる。加えてリサーチの分野においても,その応用が大きく期待されるCTであると確信できる。
