大阪国際がんセンターにおけるHyperArc治療の軌跡
Varian Oncology Summit 2022
2022-12-1
座長:青山 英史(北海道大学大学院医学研究院放射線科学分野放射線治療学教室)
-
大阪国際がんセンターにおけるHyperArc治療の軌跡:技術編
宮崎 正義(大阪国際がんセンター放射線腫瘍科) -
大阪国際がんセンターにおけるHyperArc治療の軌跡:臨床編
小西 浩司(大阪国際がんセンター放射線腫瘍科)
大阪国際がんセンターにおけるHyperArc治療の軌跡:技術編
宮崎 正義(大阪国際がんセンター放射線腫瘍科)

当センターでは2019年5月に,バリアン社の放射線治療装置「TrueBeam」に“HyperArc”を導入した。国内で最も多くのHyperArcを実施している経験を踏まえ,HyperArcの付加価値を提案するとともに,本邦初稼働となった「TrueBeam Edge」の精度検証の結果などを紹介する。
HyperArcの頭頸部領域への応用
HyperArcは,主に転移性脳腫瘍に対する定位手術的照射を短時間かつ効率的に行えるソリューションであるが,当センターでは,危険臓器の線量低減や照射時間短縮が期待できるnon-coplanar照射をさらに活用したいと考え,頭頸部領域のがんに応用している。
第4頸椎への定位照射を行った症例では,coplanar照射に比べてHyperArcでは20% isodoseラインが小さく,線量が集中していた。線量体積ヒストグラム(DVH)でも,喉頭や顎下腺の線量低減が確認された。同様に頸部リンパ節転移症例においても,HyperArcでは20% isodoseの範囲が小さく,DVHでは口腔や咽頭収縮筋の線量が低減されており,ターゲットに近い同一断面の危険臓器の線量低減に非常に有用であった。
また,HyperArcはcoplanar強度変調回転放射線治療(VMAT)とのハイブリッド照射が可能である。上咽頭がんの症例(図1)では,イニシャルプランはcoplanar 2arcのVMATで50.6Gy,ブーストプランはHyperArcで19.8Gyを照射した。ブーストプランでは,計画標的体積(PTV)に近い口腔,右耳下腺などへのさらなる線量低減が可能で,照射範囲が小さいためフラットニングフィルタフリービーム(FFF)を用いて照射時間を短縮することもできた。
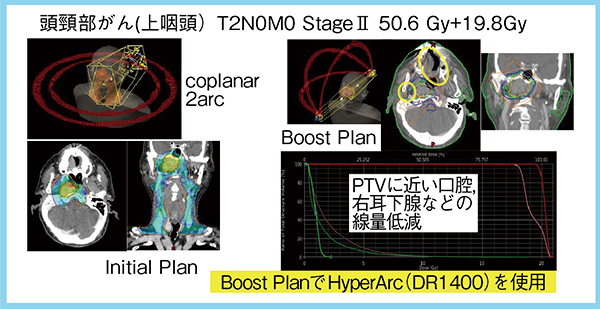
図1 上咽頭がん症例へのHyperArcの応用
HyperArcの3つの利点
1.正常脳の大幅な線量低減
当センターで,転移性脳腫瘍を対象にcoplanar VMATとHyperArcの線量を比較検討した結果,HyperArcでは正常脳で線量を受けた領域(V4Gy〜V16Gy)のボリュームが有意に減少した1)。
また,正常脳の線量低減に有用な線量計算オプション“SRS-NTO”(図2)を用いることで,線量集中性が向上し,複数個の転移性脳腫瘍においてisland blocking problemが生じないという利点が得られる。これは,SRS-NTO内部の3つのRing構造により強力に脳線量を低減できること,また,ターゲット間で処方線量の17%を超える線量のつながりを防止することで可能になっている2)。
さらにHyperArcでは,正常脳の線量低減に有効なcollimator angleの自動最適化も搭載されており,手動での設定よりも適切なcollimator angleを設定できる。当センターの検討ではV12Gy〜V16Gyのボリュームが有意に減少し,MU値も減少した3)。
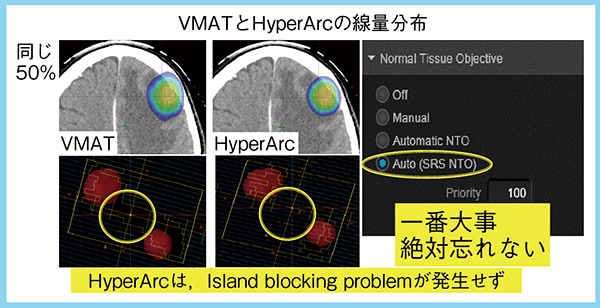
図2 SRS-NTOの有用性
2.寝台自動移動
従来のnon-coplanar照射では,寝台移動のために,その都度操作者が治療室に入って操作する必要があったが,HyperArcでは寝台を遠隔操作できるため治療時間の短縮につながる。
3.治療時間の短縮
HyperArcでは多発症例でも1 isocenterで治療が可能なため,患者の入室から退室までが約20分と短く,患者の負担を軽減できる。また,治療においては,治療前後にcone beam CT,照射・回転ごとにlinac graphy(LG)を撮影し,治療計画と照合することで照射精度を担保している。
TrueBeam Edgeの精度検証
TrueBeam Edgeは定位放射線治療に特化したリニアックで,HyperArc が標準搭載されている。2019年9月に本邦で初めて当センターに導入され,12月より稼働を開始した。TrueBeamではQA支援ツール“Machine Performance Check(MPC)”を使用できる。MPCとchamberで測定した出力のトレンドが一致していることを確認し,MPCでDaily QAを実施している。出力変動は1%以内を基準としており,3か月に1回の校正を行っている(図3)。
位置精度については,導入時と導入1年後でLutzテストの結果を比較したところ,おおむね0.5mm以内の精度を確認でき,経時変化はほぼ見られていない。
また,TrueBeamとTrueBeam Edgeの2台について,寝台とビーム中心の誤差を日々のMPCの結果で確認したところ,装置間の位置誤差は0.5mm以内,角度は0.1°以内であった。
さらに,マルチリーフコリメータ(MLC)幅の影響を検証した。直径5mmのPTVに対して2.5mmと5mmのMLC幅で線量分布を比較すると,2.5mm幅の方が正常組織への線量を低減できた。小さいターゲットには小さいMLCが適していると言える。
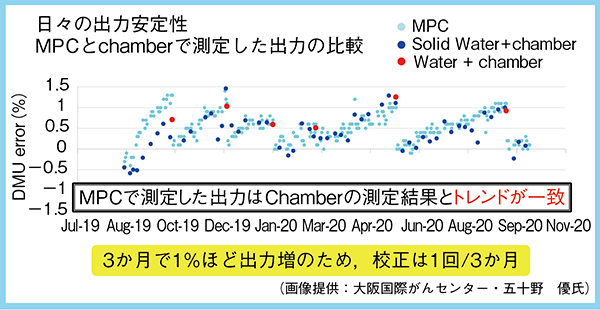
図3 MPCとchamberで測定した出力の比較
●参考文献
1)Ohira, S., et al., Radiat. Oncol., 13(1),13, 2018.
2)Clark, G.M., et al., Pract. Radiat. Oncol., 2(4),306-313, 2012.
3)Ohira, S., et al., Med. Dosim., 45(1),85-91, 2020.
大阪国際がんセンターにおけるHyperArc治療の軌跡:臨床編
小西 浩司(大阪国際がんセンター放射線腫瘍科)

本講演では,HyperArcの特長と当センターにおける多発脳転移に対する定位放射線照射(STI)の現状を報告する。
HyperArc導入の背景
多数個の転移性脳腫瘍の治療選択について,『脳腫瘍診療ガイドライン 2016年版』では,「推奨1 全脳照射を行う」「推奨2全脳照射にSTIを加えてもよい」「推奨3 腫瘍の薬物療法感受性によっては薬物療法を行ってもよい」「推奨4 機能予後あるいは生命予後の改善が期待される場合には腫瘍摘出術を行ってもよい」と記載されており,この時点ではSTI単独治療は推奨されていなかった。
ところが近年,薬物療法の進歩などにより,脳転移があっても長期生存する患者が増加し,全脳照射による晩期障害が問題視されるようになってきた。全脳照射後2年で高度な認知機能の低下が見られるという報告1)や,全脳照射開始後6か月でも認知機能が低下するとした報告2)もある。また,脳のSTIに関する臨床試験(JLGK0901:STI単独治療)の結果として,脳転移の数が2〜4個と5〜10個で全生存期間に差はないと報告されており3),多数個の脳転移に対してSTI単独治療が試みられるようになってきた。
これらの結果を受けて,『脳腫瘍診療ガイドライン 2019年版』では,新たに「推奨5 腫瘍の個数,体積の合計,照射回数を十分に考慮し,厳重なフォローアップを前提にSTI単独治療を行ってもよい」が追加され,さらに,脳転移が11〜15個でも生存率に差がないことが報告4)されたことで,現在,STIの役割はより大きくなっている。
HyperArcの特長と当センターでのSTIの現状
当センターは,2017年に大阪府立成人病センターから大阪国際がんセンターに名称変更を行った。当時はTrueBeam 2台と「TrueBeam STx」1台の3台で治療を行っており,脳転移に対してはTrueBeam STxを駆使してVMATにてSTIを行っていたが,5個以上の多数個の転移症例については,ガンマナイフなどが稼働する施設に紹介していた。その後,2019年にTrueBeam STxにHyperArcを搭載し,さらに同年,HyperArcを内蔵したTrueBeam Edgeを導入して,2台の装置でHyperArcを実施可能となった。これにより,1台が故障しても,もう1台の装置でHyperArcを行えるという利点がある。また,HyperArcは,2°ごとにリーフを変えられるため,non-coplanar beamのコントロールポイントの総数は442,つまり442方向から腫瘍をねらい撃ちすることができる(図1)。ガンマナイフなどと遜色のない線量分布での治療を,より短時間で行えることも利点である。
HyperArcを導入後,当センターでは脳のSTI単独治療の件数が増加しており,2021年には200症例を超えた。原発巣別の内訳は,肺がんが最も多く60%を占め,乳がん,胃がん,腎がん,食道がんと続く。5個以上の多発脳転移に対しても積極的にSTI単独治療を行っており,転移個数別の内訳で5個以上の症例が占める割合は,HyperArcを開始した2019年は23%であったが,2021年には42%に増加した。また,STI単独治療では,治療してない部位からの再発や新規脳転移が発生するが,それに対してもSTIを実施しており,なかには5回以上の治療を行っている症例もある。
当センターの約150症例,合計約250個の病変に対する脳STIの成績を解析したところ,6か月後に65%以上あるいは90%以上の病変の縮小が見られた症例は,65%未満あるいは90%未満の症例と比較して有意に局所制御が良好であった。また,6か月後に65%以上あるいは90%以上の病変の縮小を達成するために,肉眼的腫瘍体積(GTV)D80>58Gy(BED20)が良好な予後因子であった5)。そこで,当センターでは,HyperArc導入当初は70〜80% isodose処方を採用し,GTVの最大線量は125〜140%までとしていたが,それでは線量が不十分で局所制御が不良であったため,現在は50% isodose処方としてGTV内の最大線量が200%以上となるような線量分布を作成している。

図1 HyperArcのビーム本数
HyperArcの脳転移以外への適応
当センターでは,HyperArcを頭蓋底腫瘍(図2)や頭頸部がん(図3)にも適応している。頭頸部がんにおいては,HyperArcを用いた強度変調放射線治療(IMRT)を行っているが,VMATと比較し,口腔や耳下腺の線量をよりシャープに低減できており,HyperArcはリスク臓器(OAR)の線量低減に非常に有用である。
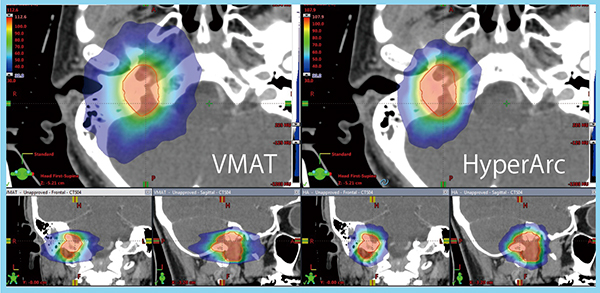
図2 頭蓋底腫瘍へのHyperArcの適応
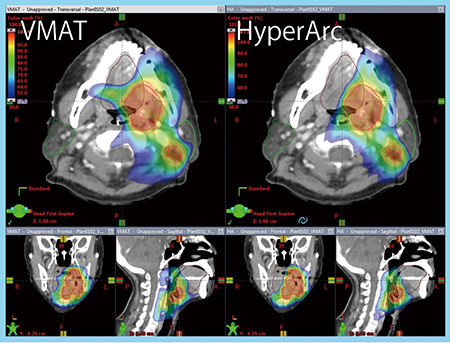
図3 頭頸部がんへのHyperArcの適応
●参考文献
1)Aoyama, H., et al., Int. J. Radiat. Oncol. Biol. Phys., 68(5) : 1388-1395, 2007.
2 )Brown, P.D., et al., Lancet Oncol., 18(8) : 1049-1060, 2017.
3)Yamamoto, M., et al., Lancet Oncol., 15(4) : 387-395, 2014.
4)Hughes, R.T., et al., Int. J. Radiat. Oncol. Biol. Phys., 104(5) : 1091-1098, 2019.
5)Kanayama, N., et al., Cancer Med., 00 : 1-10, 2022.
TrueBeam 医療用リニアック:医療機器承認番号 22300BZX00265000
放射線治療計画用ソフトウェア Eclipse:医療機器承認番号 22900BZX00265000
