メドトロニック,ラジオ波焼灼療法で用いる「Cool-tip RFAシステム Eシリーズ」が早期乳がんへの使用で新たに保険適用を取得
― 切らない早期乳がん治療という新しい選択肢 ―
2023-12-4
日本におけるメドトロニックの3法人のひとつであるコヴィディエンジャパン(株)は,「Cool-tip RFAシステム Eシリーズ」の早期乳がん1への使用に関する薬事承認を2023年7月7日に取得し,同製品は同年12月1日より保険適用となった。これにより,早期乳がんに対するラジオ波焼灼療法による治療が可能になる。

(販売名:Cool-tip RFAシステム Eシリーズ / 医療機器承認番号:22300BZX00335000)
製造販売元:コヴィディエンジャパン(株)
今回の保険適用は,先進医療制度下で実施した医師主導特定臨床研究「早期乳癌へのラジオ波熱焼灼療法の有効性の検証と標準化に向けた多施設共同研究(RAFAELO試験)」(国立がん研究センター中央病院含む国内9施設:国立研究開発法人日本医療研究開発費「標準的乳がんラジオ波熱焼灼療法確立のための多施設共同研究班」研究代表者 木下貴之)の成果によるもの。
乳がんは,年間約97,000例が診断されており2,女性における乳がんの罹患者数は,他のがんと比べて最も多いと言われている。乳がんの治療は,遠隔転移をしていることが明らかな場合を除き,手術によってがんを切除することが一般的。がんの状態によっては,手術,放射線治療,薬物療法を組み合わせて治療する3が,主な手術としては,乳房部分切除術や,乳房全切除術が挙げられる。
Cool-tip RFAシステム Eシリーズは,ラジオ波焼灼療法という,ニードル電極を腫瘍の内部に挿入し,ラジオ波帯の電気を流すことで生じるジュール熱によって,がん病変等の組織を凝固・焼灼させる治療法に用いる医療機器。2011年の発売以降,肝腫瘍に対する治療に使用されており,2018年に無心体双胎における無心体への血流遮断,2022年に小径腎悪性腫瘍及び標準治療に不適・不応の肺悪性腫瘍,悪性骨腫瘍,類骨骨種,骨盤内悪性腫瘍,四肢,胸腔内及び腹腔内に生じた軟部腫瘍へと適応を拡大してきた。
今回,Cool-tip RFAシステム Eシリーズが早期乳がんへ適応を拡大したことによって,ラジオ波焼灼療法による,乳房を切ることのない低侵襲な治療選択肢が新たに加わった。
今回の早期乳がんへの適応の拡大について,東京医療センター 副院長及び日本乳癌学会理事の木下貴之氏は,「ラジオ波焼灼療法は他の臓器において,切除不能の場合や腫瘍の一部に対して等の緩和的な要素が少なからずありますが,乳腺腫瘍(早期乳がん1)においては治癒を目的としています。適応対象を1.5cm以下,腋窩リンパ節転移及び遠隔転移を認めない限局性早期乳がんと定め,臨床試験を重ねた結果が実を結び,早期乳がんへの適応が拡大されたことを誇りに思っております。」と述べている。
今後は,早期乳がんへの使用に対する適正使用指針を満たした施設及び術者において,順次治療が可能になる。
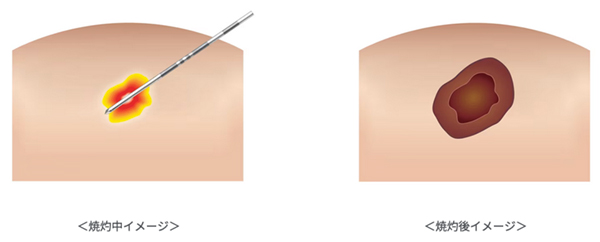
【ラジオ波焼灼療法(Radio Frequency Ablation : RFA)とは】
ラジオ波焼灼療法とは,ニードル型の電極を腫瘍の内部に挿入し,ラジオ波帯(約472KHz)の電流を流すことで生じるジュール熱によって,がん病変組織等を凝固・焼灼させる治療法。
【RFA治療適用の早期乳がんについて】1
今回の早期乳がんへの適応拡大における治療の対象は,腫瘍径 1.5 cm以下の単発,触診及び画像診断による 腋窩リンパ節転移及び遠隔転移を認めない限局性早期乳がんとなる。
【RAFAELO試験(NCCH1409試験)について】
本試験は腫瘍の大きさが 1.5 cm以下の単発,触診及び画像診断による 腋窩リンパ節転移及び遠隔転移を認めない限局性早期乳がんの患者を対象にCool-tip RFAシステム Eシリーズを用いたRFAの有効性・安全性を評価する第III相医師主導特定臨床研究(詳細については臨床研究実施計画・研究概要公開システム[jRCT,https://jrct.niph.go.jp/latest-detail/jRCTs032180229
]参照)。
「標準的乳がんラジオ波熱焼灼療法確立のための多施設共同研究」の研究班(研究代表者 木下貴之 現 国立病院機構 東京医療センター)の計画のもと,国立がん研究センター中央病院を中心に,同院など全国9施設で,372名の患者が参加した。
本試験の短期成績における乳房内無再発生存割合は標準治療である乳房部分切除術に劣らない成績であった。
本試験を実施した医療機関
・国立病院機構北海道がんセンター
・群馬県立がんセンター
・千葉県がんセンター
・国立研究開発法人国立がん研究センター東病院
・国立研究開発法人国立がん研究センター中央病院
・岡山大学病院
・広島市立病院機構広島市立広島市民病院
・国立病院機構四国がんセンター
・岐阜大学医学部附属病院
【特定臨床研究とは】
「臨床研究」とは,医薬品等を人に対して用いることにより,当該医薬品等の有効性又は安全性を明らかにする研究(当該研究のうち,当該医薬品等の有効性又は安全性についての試験が,医薬品,医療機器等の品質,有効性及び安全性の確保等に関する法律(昭和 35 年法律第 145 号。以下「医薬品医療機器等法」という。)第 80 条の2第2項に規定する治験に該当するものその他厚生労働省令で定めるものを除く。)をいう。(第2条第1項関係)
「特定臨床研究」とは,臨床研究のうち,次のいずれかに該当するものをいう。(第2条第2項関係)
(ⅰ) 医薬品等製造販売業者又はその特殊関係者(医薬品等製造販売業者と厚生労働省令で定める特殊の関係のある者をいう。以下同じ。)から研究資金等(臨床研究の実施のための資金(厚生労働省令で定める利益を含む。)をいう。以下同じ。)の提供を受けて実施する臨床研究(当該医薬品等製造販売業者が製造販売をし,又はしようとする医薬品等を用いるものに限る。)
(ⅱ) 未承認医薬品等(医薬品等であって,医薬品医療機器等法の製造販売の承認若しくは認証を受けていないもの又は届出が行われていないものをいう。)又は適応外医薬品等(医薬品等であって,医薬品医療機器等法の製造販売の承認若しくは認証を受けているもの又は届出が行われているもの(当該承認,認証又は届出に係る用法,用量,使用方法その他厚生労働省令で定める事項(以下「用法等」という。)と異なる用法等で用いる場合に限る。)をいう。)を用いる臨床研究((ⅰ)に該当するものを除く。)
「医薬品等」とは,次に掲げるものをいう。(第2条第3項関係)
(ⅰ) 医薬品医療機器等法第2条第1項に規定する医薬品(同条第14 項に規定する体外診断用医薬品を除く。)
(ⅱ) 医薬品医療機器等法第2条第4項に規定する医療機器
(ⅲ) 医薬品医療機器等法第2条第9項に規定する再生医療等製品
「医薬品等製造販売業者」とは,医薬品等に係る医薬品医療機器等法 の製造販売業の許可を受けている者をいう。(第2条第4項関係)
(臨床研究法の公布について(平成29年4月14日医政発0414第22号厚生労働省医政局長通知))
【先進医療とは】
先進医療については,平成16年12月の厚生労働大臣と内閣府特命担当大臣(規制改革,産業再生機構),行政改革担当,構造改革特区・地域再生担当との「基本的合意」に基づき,国民の安全性を確保し,患者負担の増大を防止するといった観点も踏まえつつ,国民の選択肢を拡げ,利便性を向上するという観点から,保険診療との併用を認めることとしたものです。また,先進医療は,健康保険法等の一部を改正する法律(平成18年法律第83号)において,「厚生労働大臣が定める高度の医療技術を用いた療養その他の療養であって,保険給付の対象とすべきものであるか否かについて,適正な医療の効率的な提供を図る観点から評価を行うことが必要な療養」として,厚生労働大臣が定める「評価療養」の1つとされています。 具体的には,有効性及び安全性を確保する観点から,医療技術ごとに一定の施設基準を設定し,施設基準に該当する保険医療機関は届出により保険診療との併用ができることとしたものです。
(厚生労働省HPより引用)
参考ページ
先進医療の概要について
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou_iryou/iryouhoken/sensiniryo/index.html
臨床研究法について
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000163417.html
1 Cool-tip適用対象となる乳がん
2 全国がん罹患データ 2019年 参照
3 がん情報サービス 参照
●問い合わせ先
日本メドトロニック(株)
www.medtronic.co.jp
