セミナーレポート(富士フイルムヘルスケア)
Ultrasonic Week 2019が,2019年5月24日(金)〜26日(日)の3日間,グランドプリンスホテル新高輪(東京都港区)にて開催された。24日に行われた株式会社日立製作所共催のランチョンセミナー4では,埼玉医科大学国際医療センター心臓内科教授の岩永史郎氏を座長に,筑波大学医学医療系循環器内科学臨床検査医学病院教授の石津智子氏と東北大学病院生理検査センター生理検査部門長の三木俊氏が,「精度の高い心血管エコー検査を目指して─見逃せない心不全と動脈硬化のサイン」をテーマに講演した。
2019年9月号
Ultrasonic Week 2019ランチョンセミナー4 精度の高い心血管エコー検査を目指して ─見逃せない心不全と動脈硬化のサイン
精度の高い心血管エコー検査を目指して─見逃せない動脈硬化のサイン
三木 俊(東北大学病院生理検査センター)
日立製の超音波診断装置「LISENDO 880」には,全身の血管に対する形態,動態,機能のより詳細な把握を可能とするさまざまなアプリケーションが搭載されており,それらを“血管パッケージ”として提供している。本講演では,血管病変を早期にとらえるのに有用な機能を紹介する。
血管マネージメントシステムによる早期動脈硬化の予防と診断
血管マネージメントシステムとして,器質的変化の各段階におけるそれぞれの機能の活用を紹介する。
1.1st stage:血流依存性血管内皮機能(FMD)検査
日立製の超音波診断装置は,汎用機としては唯一,自動FMD(Flow Mediated Dilation)解析が可能である。固定アームで腕を固定して,上腕あるいは前腕を数分間駆血し,解放後の血流増加による血管拡張反応を観察して血管内皮機能を評価する。%FMDのほか,脈波増大係数(AI)やピーク血流速度,血流量など,さまざまな指標を算出可能である。
2.2nd stage:血管弾性評価(eTRACKING)
“eTRACKING”は,トラッキングゲートが拍動による血管壁の動きを自動的に追従し,血管径変化を高い精度でリアルタイムに計測する機能である。自動で算出される動脈硬化の複数の指標のうち,Stiffness Parameter βは血圧依存性が少なく,信頼性が高い。Stiffness Parameter βは局所の硬さの指標であり,総頸動脈で計測することが多い。ガイドラインでは明確な基準値は示されていないが,13以下が正常と判断される。
3.3rd stage:血管壁肥厚評価(Auto IMT)
mean IMT(平均内中膜厚)について,日本超音波医学会の新しいガイドライン1)では,一定の範囲を自動トレースし,1cmの範囲で100点以上のIMTの平均を自動計測する方法が示されている。“Auto IMT”は,血管の長軸断層像に関心領域(ROI)を設定するだけで,IMTの抽出と100点以上のIMTの計測を自動で行い,定量化することができる。
4.4th stage:血流評価(リニアST-CWドプラモード)
リニアST-CWドプラモード(Linear CW)では,リニアプローブでの連続波(CW)ドプラ走査が可能であり,セクタプローブに持ち替えることなく高速血流を評価することができる。実際の高度狭窄の症例では,388.5cm/sの超高速な血流を評価可能であった(図1)。
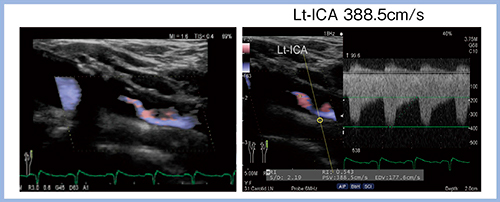
図1 リニアST-CWドプラモードによる高速血流の評価
5.5th stage:血管内皮機能の観察(VFM Vascular)
LISENDO 880に新たに搭載された“VFM(Vector Flow Mapping)Vascular”では,壁面剪断応力(wall shear stress:WSS)の観察が可能である。WSSの観察により血管内皮機能を予測できる可能性や,血管内皮機能と心不全とのかかわりなどが注目されており,VFM Vascularへの期待も大きい。VFM Vascularでは,3心拍のWSSを測定し,その平均値を算出する(図2)。今後の可能性については後述する。
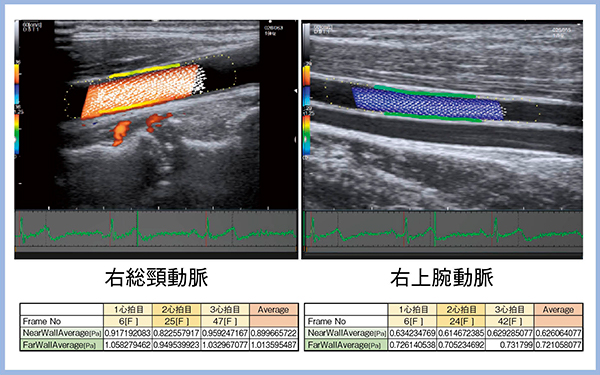
図2 VFM VascularによるWSSの観察
簡便で正確な下肢動脈検査のための血管パッケージ
1.Protocol AssistantとiVascular
“Protocol Assistant”は,検査プロトコールをあらかじめ登録できる機能である。検査中のボタン操作などの手間を大幅に削減できるほか,画面上に検査項目が一覧でわかりやすく表示されるため,客観的かつ取りこぼしのない検査を短時間で効率良く行うことができる(図3)。
“iVascular”は,カラードプラの関心領域,カーソルの位置・幅・補正角度の4つの設定がワンボタンで自動的に調節される機能で,理想的なパルス波形が描出される(図4)。Protocol Assistantと組み合わせることで検査時間を大幅に短縮できる非常に優れた機能である。
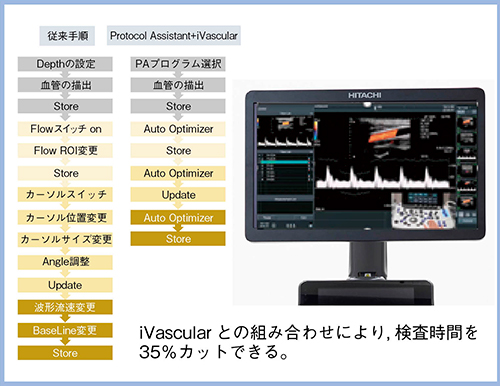
図3 Protocol Assistantの概要
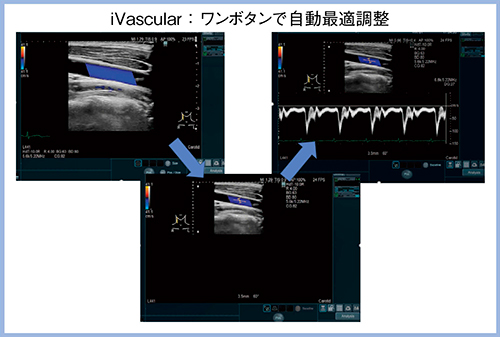
図4 iVascularの表示画面
2.Transit time of Vessel Flow(TVF)
TVFは,大腿,膝窩および足部の各動脈で得られた血流波形出現時間を測定して,得られる計測値の遅延から閉塞病変や狭窄の有無と範囲を推定できる指標である。従来は,総大腿動脈(CFA)と膝窩動脈(POP)の血流のピークの時間差などを算出して評価していたが,LISENDO 880では3心拍を自動で取り込んで簡便に評価可能となった(図5)。
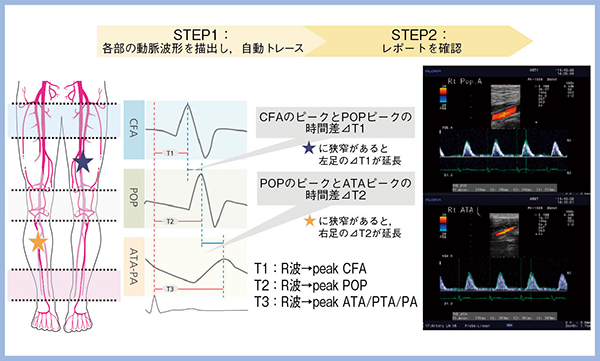
図5 自動TVF測定機能
3.Dual Gate Doppler
下肢動脈検査における収縮期最大血流速度比(PSVR)は,パルスドプラ(PW)法を用いて,まず狭小化部位の中枢側で血流速度を測定し,次に極小化部位の収縮期最大血流速度(PSV)を測定して,手動計算にて算出する。一方,“Dual Gate Doppler”では,同一心拍にてサンプルゲートを2か所設定し,同一画面上で同時に血流速度波形を評価できるため,PSVR測定が容易となり(図6),精度向上にも貢献する。
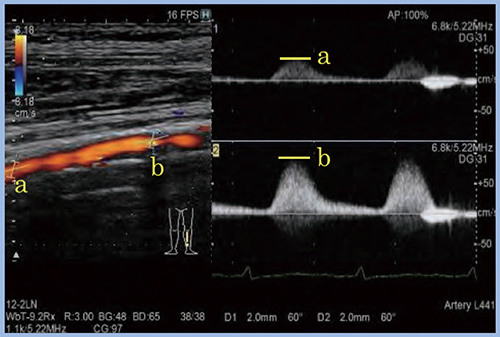
図6 Dual Gate Dopplerを用いたPSVRの測定
4.VFM Vascular
心エコーのVFMを血管に応用したVFM Vascularは,速度推定の原理を用いて真の血流方向と速度を算出し,WSSを数値化する機能である。粒子画像流速測定法(PIV)システムと,VFM Vascularのデータからそれぞれ求めたWSSを比較し精度を検証したところ,非常に高精度であったと報告されている2)。
VFM Vascularを用いた血管内皮機能の評価として,当大学にて,(1) 患者にニトログリセリンを投与することなく血管平滑筋障害を判定可能か,(2) FMD検査前に動脈硬化を判定可能か,について検討を行った。対象は,腹部大動脈瘤(AAA),末梢動脈疾患(PAD),がんの患者である。%FMDについて,AAAとがんはPADよりも低値であった。また,ニトログリセリン誘発性内皮依存血管拡張反応(%NMD)についてAAAとPADを比較したところ,AAAの方が低値であった。WSSを見ると,健常例と比較して,AAA,PAD,がんの患者は低値であり,WSSが悪化しているのは明らかであった。一方,WSSと%FMDおよび%NMDの間には,症例数が少ないこともあり相関は見られなかった。
さらに,PADとAAAのFMDおよびNMDについて,より詳細な解析が可能なトレンド解析を行い,拡張時間の違いについて検討したところ,NMDでの拡張時間および拡張時定数はAAAの方がPADより延長しており,血管平滑筋障害の可能性があると考えられた。このトレンド解析の結果とWSSとの相関を見ると,拡張時間と拡張面積についてはある程度の傾向が見られ,平滑筋の機能に関与している可能性が推測された。
5.2D Tissue Trackingを用いた検討
心エコーの“2D Tissue Tracking”を用いて,血管の長軸方向の伸縮率を算出可能か検討を行った。PADおよびAAAの患者は,健常例と比較していずれも伸縮率が非常に低下しており,長軸方向の伸縮率は動脈硬化を反映していると考えられた。また,長軸方向と短軸方向ではどちらが先に伸展するのかを検討したところ,健常例とPADはピークにズレがないが,AAAでは短軸方向の後に長軸方向が進展し,時相が少しずれていた。これが何を意味するかは現状では不明であるが,血管の平滑筋,あるいは中膜などの外側の部分に影響している可能性があると考えている。
なお,この血管距離変化率と血管最大時間変化を表す機能を,今後は“Vascular Mechanical Change”(VMC)と呼称していきたい。
まとめ
日立製超音波診断装置は,動脈および心血管の疾患の早期発見および評価に大きく貢献していると言える。全身の血管の形態・動態・機能のより詳細な把握が可能であり,VFM VascularやVMCがもたらす新たな血管の機能的評価は,今後臨床に貢献できる可能性があると期待している。
●参考文献
1)日本超音波医学会:超音波による頸動脈病変の標準的評価法2017.
https://www.jsum.or.jp/committee/diagnostic/pdf/jsum0515_guideline.pdf
2)Shimizu, M., et al., Jpn. J. Appl. Phys., 56・7S1, 07JF08, 2017.

三木 俊(Miki Takashi)
1993年 日本医療学院臨床検査学科卒業。同年 岸和田徳洲会病院検査部。2003年 徳島赤十字病院検査部。2006年
八尾市立病院検査部係長。2012年~東北大学病院生理検査センター生理検査部門長。2013年~同大学医学部保健学科臨地准教授。
- 【関連コンテンツ】
