セミナーレポート(富士フイルムヘルスケア)
第28回日本乳癌学会学術総会が2020年10月9日(金)〜31日(土)の日程でWeb開催された。株式会社日立製作所の共催セミナー53では,静岡県立静岡がんセンター乳腺画像診断科兼生理検査科部長の植松孝悦氏を座長に,愛知医科大学外科学講座乳腺・内分泌外科教授 / 同大学病院副院長兼卒後臨床研修センター長の中野正吾氏と同大学病院中央放射線部の清水郁男氏が,「Real-time Virtual Sonography(RVS)『知って得する,RVS fusion技術 ストレスフリーのセカンドルックUS』」をテーマに講演した。
2020年12月号
第28回日本乳癌学会学術総会共催セミナー53 Real-time Virtual Sonography(RVS)「知って得する,RVS fusion技術 ストレスフリーのセカンドルックUS」
ARIETTA 850を使ったRVSの実際および多施設共同臨床研究(FUSION 02)の紹介
中野 正吾(愛知医科大学外科学講座乳腺・内分泌外科)
本講演では,現在われわれが取り組んでいる“Real-time Virtual Sonography(RVS)”(日立製)の研究内容を中心に,日立製の超音波診断装置「ARIETTA 850」を使ったRVSの実際,および新たな臨床試験の概要を報告する。
乳房MRIに関する諸問題
1.MRI-detected lesion
乳がんの広がり診断において,乳房MRIは広く用いられている。乳がん検出において高い感度を示すが,特異度は相対的に低い。このため,悪性を疑うようなMRI-detected lesion (初回マンモグラフィや超音波では同定できず,MRIにて初めて同定される病変)を認めた場合,Second-look USを行い,超音波ガイド下に組織検査を行うことが必要となる1)。
2.Second-look USの問題点
Second-look USによるMRI-detected lesionの検出率は約60%とされるが,検者間や施設間において検出率にばらつきがあること2),体位変換によって病変の位置が大きく移動すること3)が報告されている。このため,客観性や再現性を高める工夫が求められる。
RVSの臨床応用
1.RVSの精度・適応
超音波フュージョン技術であるRVSは,磁気位置センサを用いて超音波画像と超音波プローブの走査面に一致したMRI/CT画像を同一モニタ上でリアルタイムに表示できる技術であり,日立が世界で初めて開発に成功した(図1)。
RVSを用いて異なるモダリティの画像比較を行うためには,同一検査体位での画像情報が必要となる。そこで,われわれは,まず腹臥位MRIを撮像し,RVSが必要な症例に対してのみ仰臥位MRIを追加して,超音波と同期させる方法を考案した4)。また,位置合わせは乳頭を同期点としている。われわれは,RVSの初期使用経験として,マンモグラフィ,超音波,MRI,MRI-RVSの主病巣検出率を比較したところ,RVSはMRIやUSと同等以上の検出率を有することを示した5)。また,RVSの位置精度について,同期点での位置同期後に超音波とMRI構築像の位置ズレを計測したところ,3Dポジショニングエラーとして12mmの精度で超音波プローブを病変に誘導できることを報告した6)。
なお,乳腺画像診断におけるRVSの主な適応は,超音波単独では描出が困難なMRI-detected lesionの検出や,non-mass enhancement (NME)のMRI造影域が超音波所見で確認できない場合などが挙げられる。
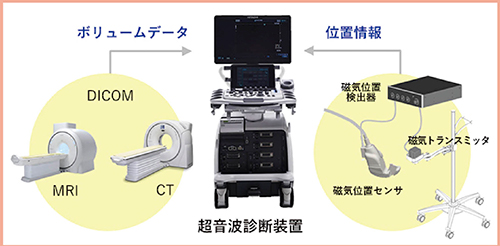
図1 Real-time Virtual Sonography (RVS)
(日立製作所ホームページより引用)
2.Second-look USへの応用と限界
RVSを用いることで,客観的に再現性を確認しながらMRI-detected lesionに超音波プローブを誘導できるため,超音波ガイド下生検が可能となる。
2011〜2015年に当科での腹臥位MRIにて同定されたMRI-detected lesion 39症例を対象に,仰臥位MRIを追加し,RVSを併用したSecond-look USを行い,病変の検出率を比較した。その結果,RVSを用いることで85%(33症例)のMRI-detected lesionに対して組織検査が施行でき,そのうち24%(8症例)に悪性病変を認めた。また,RVSで検出できない病変には悪性病変を認めなかった4)。
一方,RVSには,いくつかの限界も存在する。乳房は変形しやすいため,フュージョン操作には繊細な走査が求められる。また,仰臥位MRIの撮像においては,心拍動や呼吸性移動への対応として,撮像法や体位および体表コイルの取り扱いに工夫を要する。さらに,RVSの真の有効性を示すためには多施設共同前向き試験が必要となる。そこで現在,私が研究責任者を務める2つの臨床試験〔MRI-detected lesion:FUSION 01(登録終了),NME:FUSION 02(登録中)〕を行っている。FUSION 02については後述する。
ARIETTA 850によるRVSの実際
以下に,ARIETTA 850を用いてRVSを施行した症例を提示する。
症例1(図2)は,右乳房上方の乳がんに対して広がり診断目的にMRIを施行し,主病巣の乳頭側にMRI-detected lesion(↓)を認めた。通常のSecond-look USでは確認できなかったため,RVSによるSecond-look USを施行した。事前にMR画像上で病変にマーキング(図2○)しておくことで,RVSにてMRIのfocusに一致した低エコー腫瘤を容易に検出することができた(図2右)。針生検の結果は通常型上皮過形成であった。
また,RVSはPET/CTとの同期も可能である。症例2(図3)は,右腋窩にPETにてリンパ節への集積(↓)を認めた。CTでは皮質の肥厚を認めず,初回超音波では病変は不明確であったが,RVSによるSecond-look USを施行したところ,正常なリンパ皮質の部分的な肥厚が確認できた(図3右)。穿刺吸引細胞診の結果は陽性であった。
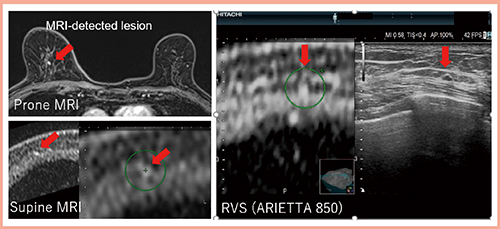
図2 症例1(72歳):主病巣の乳頭側にMRI-detected lesionを認めた症例
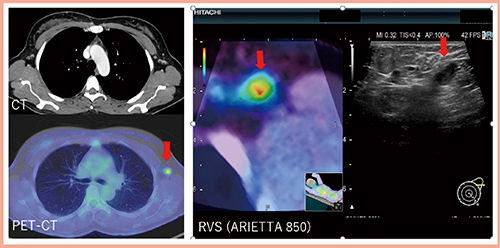
図3 症例2(38歳):PETにて右腋窩にリンパ節への集積を認めた症例
新たな臨床試験
1. NMEの広がり診断におけるRVSの有用性
MRIの造影パターンは,focus/foci,mass,NMEの3つに大別でき,このうちNMEは腫瘤の形成を伴わず,病変内に正常乳腺の介在を伴う病変と定義されている。組織型はDCISか良性病変で,focusやmassに比べ超音波での検出率が低いことや,乳房温存術においてNMEの単独病変は,mass単独やmassとmass,massとNMEに比べて再手術率が高いことが知られている7)。また,海外ではNMEに対し,MRIガイド下に造影域にフックワイヤを留置し,乳房温存術を施行するMRI-guided surgeryも試みられている8)。そこで,RVSを用いて同様のことが可能か検討を行った。
症例3は,乳房A領域にNMEを認めるが(図4左←),超音波像以上にMRIの造影域が内側に広がっているように思われた。RVSにて造影域の広がりが確認できたため(図4右■),RVSガイド下にマーキングを行い乳房温存術を施行した。主病巣はDCIS,断端は陰性であった。
当科にて,超音波よりMRI造影域の大きいNMEを有する乳がん12症例に対し,仰臥位MRIを追加して,RVSにて切除範囲を決定し,乳房温存術を施行したところ,断端陽性率は17%(2症例)であった。断端はいずれもDCISであり,再手術率は0%であった9)。
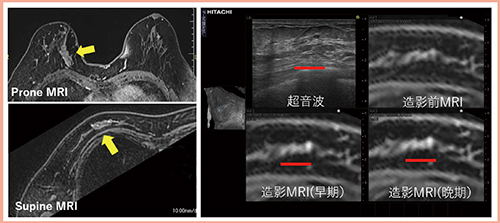
図4 症例3(68歳):乳房A領域にNMEを認めた症例
2.FUSION 02の概要
上記の結果を踏まえ,FUSION 02として,NMEを伴う病変の乳房温存術における超音波フュージョン技術の有用性を,多施設共同前向き臨床試験として検証することとした。目的は,乳房MRIにて同定されたNMEに対し,超音波フュージョン技術を用いて切除範囲を設定することが,乳房温存術の断端陽性率の改善に寄与できるかどうかを検証することである。2019年8月より症例登録を開始し,現在までに5例の登録が完了している。
まとめ
RVSを用いることで,超音波でのリアルタイムな形態画像と,MRIでの血管透過性の多寡による機能画像を直接比較・対比することが可能となる。これにより,MRI-detected lesionの検出やNMEの広がり診断に有用であった。
●参考文献
1)日本乳癌学会編:乳癌診療ガイドライン2018年版(追補2019). 99-101, 金原出版, 東京,2019.
2)Spick, C., et al., Radiology, 273(2) : 401–409, 2014.
3)Satake, H., et al., Breast Cancer, 23(1): 149-158, 2016.
4)Watanabe, R., et al., Ultrasound Med. Biol., 43(10) : 2362-2371, 2017.
5)Nakano, S., et al., Jpn. J. Clin. Oncol., 39(9) : 552-559, 2009.
6)Nakano, S., et al., Ultrasound Med. Biol., 38 (1) : 42-49, 2012.
7)Kim, O.H., et al., Breast Disease, 36(1): 27–35, 2016.
8)Kuhl, C.K., et al., Radiology, 284(3) : 645-655, 2017.
9)Ando, T., et al., Ultrasound Med. Biol., 44(7) : 1364-1370, 2018.

中野 正吾(Nakano Shogo)
1991年 熊本大学医学部卒業。同大学第二外科入局。2000年 医学博士を取得。東京大学医科学研究所附属病院外科,癌研究会附属病院乳腺外科を経て,2002年 愛知医科大学外科学講座乳腺内分泌外科。2016年 同教授。2019年 同大学病院副院長兼卒後臨床研修センター長。
- 【関連コンテンツ】
