セミナーレポート(キヤノンメディカルシステムズ)
Ultrasonic Week 2015が2015年5月22日(金)〜24日(日)の3日間にわたり,グランドプリンスホテル新高輪(東京都港区)で行われた。24日に行われた東芝メディカルシステムズ株式会社共催のランチョンセミナー12「ここにも使える ここまで診える」では,川崎医科大学検査診断学教授の畠 二郎氏を座長に,岩手県立久慈病院神経内科 リハビリテーション科医長/岩手医科大学医学部内科学講座神経内科・老年科分野助教の大浦一雅氏,京都大学大学院医学研究科人間健康科学系専攻医療検査展開学講座教授の藤井康友氏と日本大学病院消化器内科科長・超音波室室長の小川眞広氏が講演を行った。
2015年8月号
Ultrasonic Week 2015 ランチョンセミナー12 ここにも使える ここまで診える
肝疾患をSMIで診る
小川 眞広(日本大学病院消化器内科・超音波室)
超音波検査の最大の弱点は客観性が乏しいことであるが,システムの進化や撮像法の統一化により,大幅に改善されてきている。スクリーニング検査においては基本の撮像法が重要となるが,本講演では応用編として肝疾患における“Superb Micro-vascular Imaging(SMI)”を取り上げ,ピンポイントに的を絞った場合の効果を症例を提示しながら紹介する。
びまん性肝疾患
ドプラ技術の一つであるSMIは,血流のドプラ信号をプローブでとらえて血管走行を画像化する。Bモード画像上に設定したROIの血流を,造影剤を使わずに,高フレームレートで非常に高い分解能で描出することができる。さらに,ボタン1つで加算画像を作成できるため,門脈,肝動脈,肝静脈のすべての血管の構築を1画像で観察することも可能である。
肝臓の検査では主にコンベックスプローブを用いるが,高周波リニアプローブ(7MHz)を用いて肝表面近傍の血管に的を絞ることで,血管構築をSMIで高分解能に観察できる。加算画像で見ると,健常肝(図1a)の血管は比較的真っすぐ伸びているのに比べ,肝硬変症(C型)(図1b)では血管の走行が不整となり,屈曲・蛇行し,いわゆるコークスクリュー状となっている。また,門脈血低下の代償性に動脈血が増生し,表示可能な血管数の増加による血流シグナルの増加も見られ,明らかに健常肝とは血管構築が違うことがわかる。視覚的な評価には有用であり,今後,定量的,客観的な評価法が確立することを期待する。
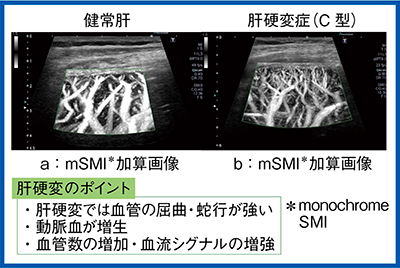
図1 健常肝と肝硬変症の血管構築の比較(mSMI加算画像)
次に,B型肝硬変症とC型肝硬変症のSMI加算画像(図2)を比較する。内部エコー以外にも血管構築の差が見られることから,今後,原因疾患による違いも検討していきたい。
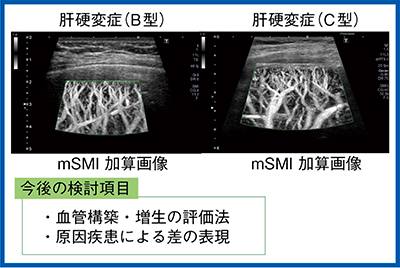
図2 原因による肝硬変症の血管構築の比較(mSMI加算画像)
肝細胞がん:TACE後局所再発
肝細胞がんで臨床的に最も問題となるのが局所再発である。TACE(肝動脈化学塞栓療法)後の塞栓した結節や近傍の淡い濃染は,CTとのフュージョン画像では容易に観察できるが,Bモード単独では把握しにくい。ただし,高エコーが欠損している部分を拾い上げることはできるため,積極的にこの部分をSMIで観察することで造影剤を使わずに局所再発の有無を確認することができる。SMI加算画像では,塞栓したボリューム内に不整血管がわずかに認められ,血流が残っていることがわかる(図3)。
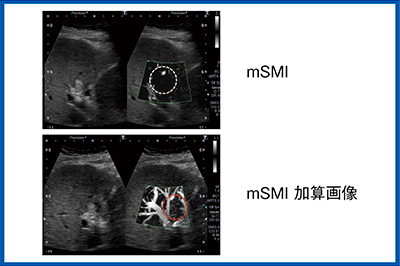
図3 肝細胞がんTACE後局所再発症例(mSMI加算画像)
そこで,造影剤を使ってさらに詳細に評価した。ソナゾイドによる造影超音波検査のポイントは,高いフレームレートで観察を行うためにROIを絞って観察をすることである。治療部位が高エコーで見えにくい場合には,造影剤の再灌流の様子を加算するMicro Flow Imaging(MFI)で造影剤が流入する場所を確認し,その部分をlow MIモードで詳細に観察する。また,輝度が低くわかりにくい場合には,2画面表示にしてBモードで関心領域を確認し,そこに注目してMFIで任意断面の濃染・血管構築を観察する。このように,目的を持って検査方法を使い分けることが大切である。
造影SMIと非造影SMIを比較する。造影することで感度が良くなり血管情報は多くなるが,ブルーミングにより血管の不整像が出現する(図4b)。一方,非造影SMI(図4a)を見ると,観察したい領域の淡い血流も描出されており,造影検査に匹敵する感度があることがわかる。細かい血流を観察するためには全体像を見るのではなく,的を絞ってROIを設定することが重要である。
なお,SMIでは腫瘍濃染像や肝実質像の評価はできないため,検査では適時造影モードとADF(Advanced Dynamic Flow)モードに切り替える準備が必要となる。腫瘍が高エコーの場合には欠損像を評価しにくいため,ADF造影の高音圧モードでの観察が必要になる。
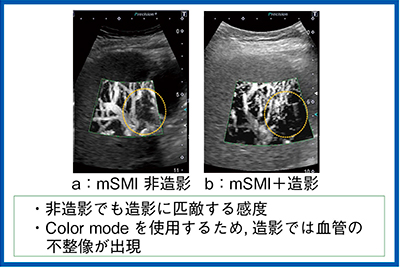
図4 SMIと造影SMIの画像比較
肝細胞がん:異所性再発
SMIは淡い微細な変化の把握に有用であるが,ROIの背景のBモードを消して血管構築を見るため,超音波検査の基本であるBモードも同時に観察できる2画面表示を推奨する。造影検査においても2画面表示とすることで,Bモードで腫瘍濃染を,SMIで不整血管を見ることができる。SMIを評価するタイミングとしては,門脈優位相と後血管相の間にSMI加算画像を取得している。従来の検査プロトコールを妨げることなく,腫瘍部の血管構築を観察することができる(図5)。
このように,SMI造影はいつでもできる利点がある。しかし,肝がんの診断には,やはり造影剤のファーストパスが最適であり,ここでも2画面表示を推奨している。ファーストパスでは,Bモード造影で腫瘍が濃染される様子と,SMIでの複雑な腫瘍血管の観察が同時に可能となるからである。そして,前述したが,気泡を再度崩壊させることにより,Bモード造影の腫瘍濃染像と,血管構築の再確認ができる。
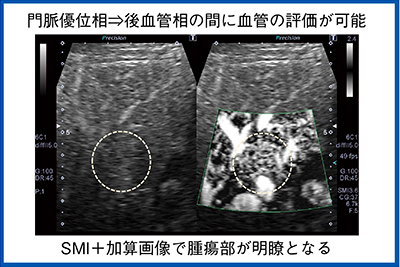
図5 肝細胞がん異所性再発
AV shunt
AV shunt(動静脈瘻)などの血管系疾患においてもSMIは有用である。造影CTで腫瘍濃染を指摘され,精査目的で受診した症例である。Bモードで淡い高エコーの近傍に門脈と太く蛇行した血管が見えることから,熟練者であればAV shuntと判断できるが,経験がないと難しい。ADFでカラー化すると動脈と肝静脈の短絡だとわかるが,CT所見の腫瘍濃染の理由がわからない。
ここで,分解能の高いSMIとBモードの2画面表示の造影検査が有用となる(図6)。ソナゾイド造影SMIの動脈優位相で,動脈と背側に流出する静脈を確認でき,Bモードでは肝実質への造影剤の漏れ出しが認められ,これがCTで確認された濃染であることがわかる。また,適時加算画像を表示することで,短絡に関与する脈管を明確に把握することが可能である。
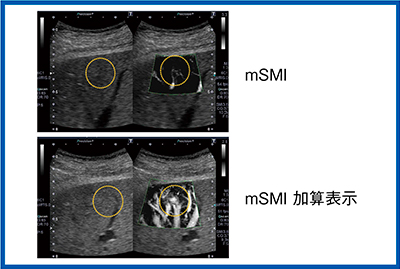
図6 AV shunt
肝細胞がんの脈管・胆管浸潤
SMIは,肝細胞がんの脈管浸潤,胆管浸潤においても有用である。門脈にも浸潤している門脈腫瘍塞栓症例において,造影モードで門脈内に黒く抜けて観察される部分が,腫瘍塞栓なのか,血栓なのかを判別するためには,再度造影剤を静注して動脈性の栄養の有無を確認する。本症例のように,動脈血の流入があれば腫瘍塞栓と考えられる(図7)。
このように,いろいろな場面でSMIは威力を発揮することがわかっていただけると思う。
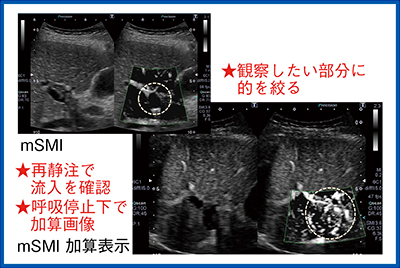
図7 肝細胞がん:門脈腫瘍塞栓症例
限局性結節性過形成(FNH)
S5に15mmの結節を指摘された症例である。MRIでは指摘できず,Bモードではかすかに低エコーの領域が見られた。明瞭なハローもモザイクパターンもないが,ADFでは低エコー領域に入る血管が認められた。これに対してROIを絞ってSMI,SMI加算画像で確認すると,低エコー領域の中心から放射状に走る腫瘍血管が観察された。さらに,造影により明瞭な腫瘍濃染と血管構築が描出され,後血管相でも欠損像を認めないことよりFNHと診断した(図8)。
図8は門脈優位相から後血管相の間に観察したものだが,SMIはこのように明瞭な放射状の血管走行をボタン1つでいつでも加算画像で確認でき,簡単に評価することができる。
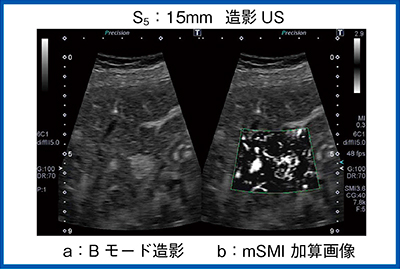
図8 限局性結節性過形成(FNH)
まとめ
肝腫瘍におけるSMIの有用性をちょっとしたテクニックとともに経験した症例で紹介した。造影剤も使えるSMIは,今後さらに肝疾患での応用が広がっていくと考えられる。

小川 眞広(Ogawa Masahiro)
1988年 日本大学医学部卒業。駿河台日本大学病院超音波室室長,日本大学医学部消化器肝臓内科講師などを経て,2008年より同医学部内化学系消化器肝臓分野診療准教授。2014年より日本大学病院消化器内科科長,超音波室室長。
- 【関連コンテンツ】
