東北大学病院,日立,日立ハイテク,がんゲノム医療のエキスパートパネル事前準備を支援するAI技術を開発
過去の治療記録や文献をもとに,医療現場の専門会議で議論すべき論点を根拠情報とともに提示
2026-3-26
東北大学病院,日立および日立ハイテクは,がんゲノム医療*1における遺伝子検査結果を医学的に解釈するための専門会議「エキスパートパネル(以下,EP)*2」の事前準備を支援するAI技術を開発した。本技術は,過去の医師コメントや関連知識,文献データベースなどを参照し,候補となりうる治療方針を含む,EPで確認・議論すべき論点を根拠情報とともに提示する*3。これにより,EPでの確認・議論が円滑化するとともに,事前準備に伴う情報収集や整理の時間が短縮され,医師の業務負担軽減に寄与することが期待される。さらに,外部に機微情報を送信しない運用を想定し,病院内のPC上で動作する仕様とした。東北大学病院の過去症例を用いた評価では,EPの検討結果と比べて,本技術が提示したEPで確認・議論すべき論点のうち,治療方針に相当する内容が8割強一致した。今後も,検証を継続しながら技術進化に努め,医療現場の負担軽減を通じて,がんゲノム医療の普及と質の向上に貢献することをめざす。
*1 がんゲノム医療: 患者ごとのがん細胞の遺伝子変異を解析し,その結果に基づいて最適な治療法を選択する個別化医療の一つ。
*2 エキスパートパネル(EP): がんゲノム医療において,患者ごとの遺伝子変異の結果をもとに,複数の専門医(腫瘍内科医,遺伝子診断医,臨床遺伝専門医,薬剤師など)が集まり,最適な治療方針や必要な追加検査について多角的に検討・助言する専門会議。個別化医療の実現を支える重要な役割を担っている。
*3 本技術の提示内容は検討のための情報であり,診断・治療方針の最終判断は医療従事者が行う。また,本技術の提示内容のみで治療方針を決定することはない。
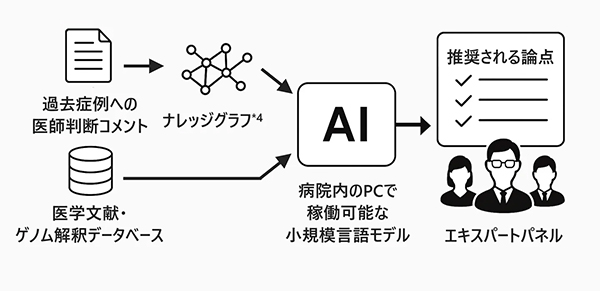
図1 EP事前準備を支援するAI技術の全体像
*4 ナレッジグラフ: 医師のコメント等から抽出した知識を関連付けて構造化し,体系的に活用できる技術。
■背景および課題
標準治療がない,または標準治療を終えた進行・再発の固形がん*5患者を対象に,がん遺伝子パネル検査(CGP)*6が2019年より保険診療として開始された。これに伴い,がんゲノム医療の対象となる患者数も2020年から2025年の5年間にかけて約2.5倍に拡大しており*7,EPで検討する症例も増加している。
一方で,EPの事前準備では,検査結果の確認に加え,関連情報の収集や検討項目の整理など多くの作業が発生する。施設や症例によっては1症例あたり最大1~2時間を要し,通常診療後に行われることもあるため,医師の業務負担が増加していることが課題であった。また,EPは専門医や分子生物学の専門家など限られた人材で運用されているため,事前準備の負担を抑えつつ,根拠情報を確認しやすい形で検討を進められる仕組みが求められていた。
*5 固形がん: 体内の臓器や組織にできる,しこり(腫瘍)として存在するがんの総称。
*6 がん遺伝子パネル検査(CGP): がん細胞のDNAを調べ,複数のがん関連遺伝子の変異を一度に網羅的に解析する検査。
*7 「がんゲノム医療とがん遺伝子パネル検査」ウェブサイト(https://for-patients.c-cat.ncc.go.jp/registration_status/
)。2020年の月平均800例程度から2025年には月平均2000例に。
■課題を解決するために開発した技術・ソリューションの特長
そこで東北大学病院,日立および日立ハイテクは,EPの事前準備に必要な情報収集・整理の効率化を支援し,候補となりうる治療方針を含む,EPで確認・議論すべき論点を根拠情報とともに提示してEPでの確認・議論を支援するAI技術を開発した。技術の特長は以下の通り。
1. 類似症例の知見を素早く参照し,事前準備の情報整理を支援
過去のEPで蓄積された医師コメントから,治療方針検討に用いられた観点や判断のポイントを抽出し,相互の関係が分かる形でナレッジグラフとして整理する。これにより,AIが類似症例で過去に議論された知見を検索・参照して医師に提示できるようになり,事前準備における情報収集・整理の効率化を支援する。
2. 医療データベースをもとに,EPで確認・議論すべき論点を根拠付きで提示
がんの種類や検査結果をもとに,CIViC*8から候補薬とエビデンスを抽出し,必要に応じてPubMed*9で関連文献も参照する。これらの情報に加え,技術1で作成したナレッジグラフもRAG*10で参照し,候補となりうる治療方針を含む,EPで確認・議論すべき論点を根拠情報とともに提示して,EPでの確認・議論を支援する。さらに,根拠が十分でない場合は無理に提案しない設計とすることで,提示内容の安全性と透明性を高める。
*8 CIViC: “Clinical Interpretation of Variants in Cancer”の略。がんに関連する遺伝子変異とその医学的意義について,世界中の専門家が情報を集めて公開しているデータベース。
*9 PubMed: 米国国立医学図書館が提供する,医学・生命科学分野の医学文献データベース。
*10 RAG: “Retrieval-Augmented Generation”の略。検索拡張生成。生成AIが回答文を作る際に,データベースや文書群から関連情報を検索(Retrieval)して取込み,その検索結果を根拠として文章を生成(Generation)する手法。モデルが学習済みの知識だけに頼らず,参照した情報に基づいて出力できるため,根拠の明確化や誤った生成(ハルシネーション)の抑制に役立つ。
3. 病院内のPCで完結した技術により機微情報を保護
機微情報の取り扱いに配慮し,病院内に設置可能なPC*11で本AIを稼働可能とするため,小規模言語モデルを用いて開発した。さらに,医師の思考ステップに合わせて処理を3段階に分けている。(1) がんの種類の特定と変異の抽出,(2) 候補薬と文献の抽出,(3) ナレッジグラフを用いたEPで確認・議論すべき論点の整理である。各段階で必要な情報だけに絞り込み,次の段階へ引き継ぐことで,入力できる情報量や処理能力に制約がある病院内PCでも必要な出力を得られるようにした。加えて,外部クラウドに機微情報を出さずに運用できるため,院内ポリシーに沿って継続利用しやすくなる。
*11 GPU搭載PC。
■確認した効果
東北大学病院でEPを実施した1,059症例のうち,1,000例を蓄積データとして活用し,残りの59症例を評価対象として,東北大学病院の医師がEPの検討結果と本技術の提示内容を照合した。その結果,EPの検討結果と比べて,本技術が提示したEPで確認・議論すべき論点のうち,治療方針に相当する内容が一致した割合は84.7%*12であった。
*12 不一致の主な要因としては日本未承認薬の推奨や本検討段階では対象外である治験情報の提供など。
■今後の展望
今後,東北大学病院,日立および日立ハイテクは,EP事前準備における業務負担軽減効果を継続して検証し,医療機関ごとの入力データ形式や運用の違いに対応した実装も検討する。がんゲノム医療連携病院など幅広い医療現場への展開も視野に,EP事前準備の効率化を通じて,がんゲノム医療の普及と質の向上に貢献することをめざす。
なお,本成果の一部は3月26日~28日に横浜で開催される第23回日本臨床腫瘍学会学術集会で発表予定。
■関連情報
●問い合わせ先
(株)日立製作所 研究開発グループ
問い合わせフォームへ
