日本メジフィジックス,アクチニウム225の小型加速器による治験薬製造スケールでの製造に世界で初めて成功
新しいがん治療と期待されるTATのコア原料
2022-4-6

創薬拠点「CRADLE棟」
日本メジフィジックス(株)は,自社の創薬拠点(*1)にてTAT(標的α線(*2)治療:Targeted Alpha Therapy)のコア原料となるアクチニウム225のGBq(*3)スケールでの製造に成功した。小型加速器を用いた,治験薬原料に利用できる品質でのアクチニウム225のGBqスケールでの製造は世界初(*4)となる。
セラノスティクス(*5)の1つであるTATは,がん細胞を死滅させるα線を放出する放射性核種を,がん細胞のタンパク質などに選択的に集積する抗体などに結合させた治療薬により,体内からがん細胞を攻撃する新しい治療概念となる。特に,α線を放出するアクチニウム225のTAT療法は,がんが全身に転移した前立腺がんの患者に対する高い治療効果が2016年に報告(*6)されて以降,世界で急速に臨床研究が進んでいる。
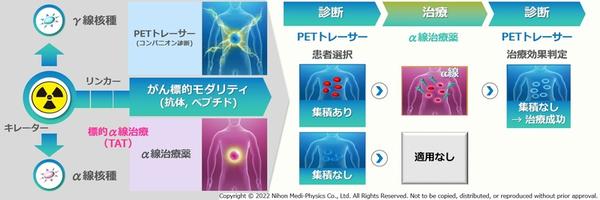
セラノスティクス概念図
そのため,天然には存在しない放射性核種であるアクチニウム225の製造開発も世界で活発に行われている。同社が開発した製造技術は,ラジウム226を原料として商業的に利用されている小型の加速器を用いる(p,2n)法(*7)で,同じラジウム226を原料とする他の製造法と比較して,ラジウム226の使用量が少量で済むなど,経済性に優れ,安定製造がしやすい方法となっている。
同社は,国立研究開発法人日本医療研究開発機構(AMED)の平成29年度 「医療研究開発革新基盤創成事業(CiCLE(*8))」(第2回)に採択された研究課題(*9)を推進することにより,セラノスティクスの早期実現を目指している。今回の製造技術の開発により,今後,自社の創薬拠点にて臨床開発に必要となる量のアクチニウム225を準備できることから,産学官で連携したTATの研究開発をさらに加速させていく。
*1:セラノスティクスの研究開発を推進するために,2019年に33億円を投資して竣工した研究施設。
*2:他の放射線に比べ,生物学的効果比が高く,飛程が短い特色をもつ。目的とする癌細胞をより強力に破壊する一方,透過力が弱いため正常組織に対する影響も最小限に抑えられ,がんを集中的に攻撃する効果の高い治療が期待できる。
*3:ギガベクレル。ベクレルは放射能の量を表す単位。*6の報告では,1人の患者に体重1kgあたり0.1メガベクレルのアクチニウム225化合物が4回投与された。
*4:2022年3月同社調べ。
*5:治療(Therapeutics)と診断(Diagnostics)を融合した造語。薬物が標的とするたんぱく質に到達するかをあらかじめ診断により確認した後に,放射性核種を治療用核種に変えて治療を行う概念。これにより,治療と診断がより密接に関連することになるため,個別化医療や医療費の有効活用への貢献が期待される。
*6:C. Kratochwil et al., J Nucl Med. 2016, vol.57, p1941-1944.
*7:加速器により高速化された陽子ビームがラジウム226原子に衝突することにより,2個の中性子が放出されアクチニウム225原子に変換される原子核反応を利用した製造方法。
*8:AMEDが推進する事業の一つで,革新的な医薬品・医療機器等の創出に向けて,政府出資を活用し,産学官が連携して取り組む研究開発を支援し,またその環境の整備を促進するもの(AMEDのホームページから)。
*9:「セラノスティクス概念を具現化するための創薬拠点整備を伴う,抗体等標識治療薬(アルファ線)とコンパニオン診断薬の開発」
●問い合わせ先
日本メジフィジックス(株)
https://www.nmp.co.jp/
