次世代の画像解析ソフトウェア(AZE)
2019年10月号
No.210 AVMにおける3D-RAのフュージョンを用いた血流識別の試み
福森 悠(医療法人翠清会 翠清会梶川病院放射線部)
はじめに
脳動静脈奇形(AVM)の治療に対しては,流入動脈(feeder),異常血管塊(nidus),流出静脈(drainer)の把握が不可欠であり,血管評価には一般的にDSA撮影が最適であると言われている。DSA画像は,カテーテルで誘導した血管からの造影血管像が描出され,平面的にしか血流動態を見ることができない。それに対し,3-dimensional rotational angiography(3D-RA)は,回転撮影の元画像をワークステーションで再構成することで,三次元的に血管を把握することができる。
しかしながら,3D-RAは選択的な撮影になるため,すべての撮影を重ねて読影することができないというデメリットが生じる。本稿では,「AZE VirtualPlace 風神」(AZE社製)を用いて,デメリットを克服した3D-RAのフュージョン画像を作成し,AVMの血管把握に有用だった例を紹介する。
3D-RAのフュージョンVR画像の作成方法
使用するDSA画像は,以下の6点である。なお,<1>と<2>,<3>と<4>はそれぞれ同一撮影である。
<1> 左内頸動脈撮影(ICAG)(ライブ像)
<2> 左ICAG(サブトラクション像)
<3> 右ICAG(ライブ像)
<4> 右ICAG(マスク像)
<5> 位置合わせ再構成後の右ICAG(ライブ像)
<6> 位置合わせ再構成後の右ICAG(サブトラクション像)
両側のICAGの3D-RAのフュージョンVR画像の作成方法は次のとおりである。なお,本稿では,DSA装置「Allura Clarity」(フィリップス社製)で撮影した<1>の3D-RAの元画像をベースとし,アプリケーションは“フュージョン”を用いた。
(1)<1>,<3>の元画像を使用し,レジストレーションに正規化相互情報量を用いて,位置合わせを行った画像<5>を作成する。ICAGでフュージョンさせる場合,重なり合う血管が少ないため,頭蓋骨を指標とした。
(2)フュージョンのアプリケーション上で<5>から<4>を「引き算」による再構成を行い,血管のみが抽出された画像<6>を作成する。
(3)<1>については,DSA装置上であらかじめ位置情報が同じ血管像が作成されているもの(<2>)に差し替える。
(4)<2>と<6>の画像を,マルチボリュームのアプリケーションで再構成し,それぞれ色分けすることで,両側ICAGのフュージョンVR画像が完成する。
症例提示
1.症例1(図1,2)
前大脳動脈(ACA)領域にnidusを有する患者。両側ICAGのフュージョンVR画像を左右の血流で色分け(右ICAGを赤,左ICAGを青)することで,左ACAメインfeederの一部に右ACAが融合していることが確認できた(図1→)。また,左ICAGのオパシティを下げることで,右ACAからnidus全体に対して流入している血管の割合が視覚的に判断しやすくなった(図2)。

図1 症例1:左右の血流色分けVR画像 |
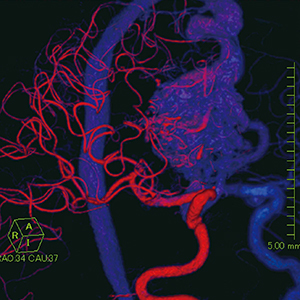
図2 症例1:左ICAGのオパシティを下げたVR画像 |
2.症例2(図3)
左側頭葉にnidusを有する患者。本症例では,左ICAGと左椎骨動脈撮影(VAG)の3D-RA画像を使用し,前述した作成方法でフュージョンVR画像を作成した。通常のDSA画像で把握困難であった後大脳動脈(PCA)の細いfeederからのnidusへの流入を確認でき,さらにMRI(脳表)・CT(骨)のフュージョンを行った後,マルチレイヤーを使用しnidus周辺の血管を色分けしたことにより,関与している血管を容易に確認でき,治療支援画像となった一例である。
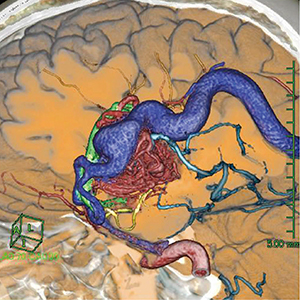
図3 症例2:マルチボリュームを用いた術前シミュレーション
PCA(水色),nidus(赤),drainer(青)
3.症例3(図4,5)
ACA領域にnidusを有する患者。両側ICAGのフュージョンVR画像を作成しても,左右から流入する血管が多く混在して見られる場合(図4 a)は,閾値を細分化したカラーマップ(図5)に置き換え,WL/WWを調整することで右中大脳動脈(MCA)の細い枝が高信号(赤)になり,feederを視覚的にとらえやすくなった(図4 b)。これは,nidusに流入した造影剤が,対側から流入する血流が多いために,nidusからdrainerにかけて急速に希釈され,feederと比べると信号値は比較的低くなるといった信号値の差を利用している。また,そのほかに,feederはnidusより先に造影されるため,信号値が若干高くなることも影響していると考えられる。
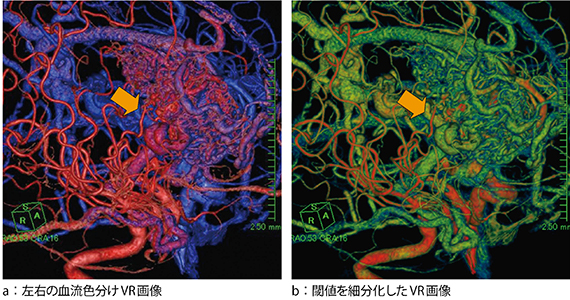
図4 症例3:両側ICAGのフュージョンVR画像
→:feeder
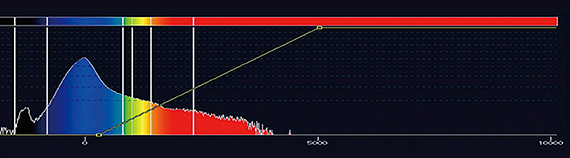
図5 症例3:閾値を細分化したオパシティカー
横軸:信号値
縦軸:オパシティ
まとめ
AVMに対する3D-RAのフュージョンVR画像は,各血管の血流動態を色分けすることにより,それぞれnidusに向かう細い血管の融合部などを明瞭に抽出することが可能である。
また,片側のICAGのオパシティを下げることで,nidus全体に対して左右からの流入割合が視覚的にとらえやすくなった。左右から流入する血管が多く見られfeederがわかりにくい場合は,閾値を細分化したカラーマップに変更することで,feederをより細かく色分けし,表現する方法が有用であった。しかしながら,これらの手法での作成症例は現在のところまだ少ないため,今後症例を重ね,3D-RAのフュージョンVR画像の有用性を検討していきたい。
【使用DSA装置】
Allura Clarity(フィリップス社製)
【使用ワークステーション】
AZE VirtualPlace 風神(AZE社製)
