セミナーレポート(キヤノンメディカルシステムズ)
第79回日本医学放射線学会総会など3学会の合同によるJRC2020が,5月15日(金)〜6月14日(日)までWeb開催された。共催セミナー11(キヤノンメディカルシステムズ株式会社)では,大阪大学大学院医学系研究科放射線統合医学講座放射線医学教室教授の富山憲幸氏の司会の下,東京医科歯科大学大学院医歯学総合研究科画像診断・核医学分野教授の立石宇貴秀氏,広島大学大学院医系科学研究科放射線診断学研究室教授の粟井和夫氏,慶應義塾大学医学部放射線科学教室教授の陣崎雅弘氏が,「最先端CTの臨床最前線」をテーマに講演を行った。
2020年7月号
第79回日本医学放射線学会総会共催セミナー11 最先端CTの臨床最前線
デジタルPET/CTの使用経験と将来展望
立石宇貴秀(東京医科歯科大学大学院医歯学総合研究科画像診断・核医学分野)
2019年10月に国産初のデジタルPET/CTとして発売された,キヤノンメディカルシステムズの「Cartesion Prime」は,デジタルPET検出器と80列CTを組み合わせたハイエンド装置として注目されている。当院では同年9月より試験的稼働を開始し,現在までに多数の症例に用いている。本講演では,デジタルPET/CTの使用経験と将来展望について,臨床例を踏まえて報告する。
Cartesion Primeの概要
1.技術的な特徴
デジタルPET/CTは,従来型検出器の光電子増倍管(photomultiplier tube:PMT)を半導体光センサ(silicon photomultiplier:SiPM)に置換したもので,Cartesion Primeでは,LYSOシンチレータで生じた可視光をSiPMにより電気信号に変換している。SiPMは,電気信号の時間的な揺らぎが小さいことが大きな特長であり1),従来のPMTやavalanche photodiode(APD)と比較して,明らかにtime-of-flight(TOF)時間分解能が向上する。これにより,Cartesion PrimeではSNRやコントラストが大幅に改善され,小さな病変も明瞭に描出可能となった。
症例1は,多発性骨髄腫である。多発性骨髄腫は18F-FDGの病変への集積が弱いことが多く,小病変の検出は難しいとされているが,Cartesion Primeでは,CT骨条件の画像では描出されない胸骨の病変部への集積が認められる(図1)。
症例2は,左乳がんである。初診時と比較して6か月後の再診時のPET/CTにて,原発巣の増大と転移巣の増加が認められた(図2)。腫大した腋窩リンパ節の一部にも集積が認められ(図2◯),腫瘍塊を形成していると考えられた。
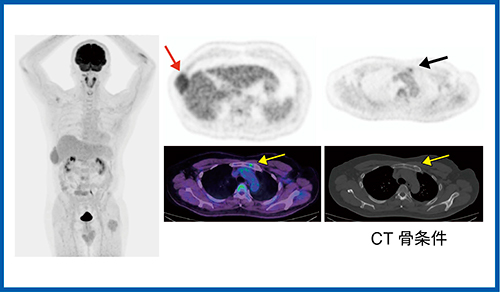
図1 Cartesion Primeによる小病変の検出
(症例1:多発性骨髄腫)
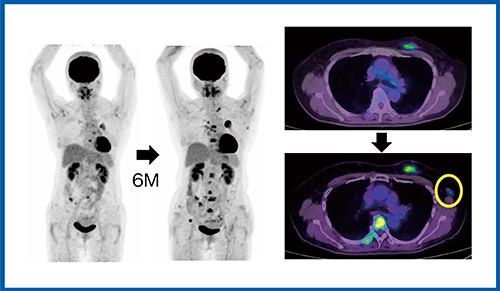
図2 Cartesion Primeによる小病変の検出
(症例2:左乳がん)
2.機種によるTOF機能の比較
Cartesion Primeと同社の「Celesteion」について,TOF-PETの機能を比較したところ,TOF時間分解能は,Celesteionの450ピコ秒以下に対してCartesion Primeでは280ピコ秒未満に改善している(いずれも保証値)。また,NEMAで定められたPETボディファントムを用いた画質評価においても,30秒/ベッドでのPET画像のコントラストノイズ比(QH, 10mm to N10mm ratio:QNR)が,Celesteionの1.66からCartesion Primeでは2.99へと明らかな画質改善が認められ,収集開始後30秒で基準値(2.8)をクリアしている(図3)。
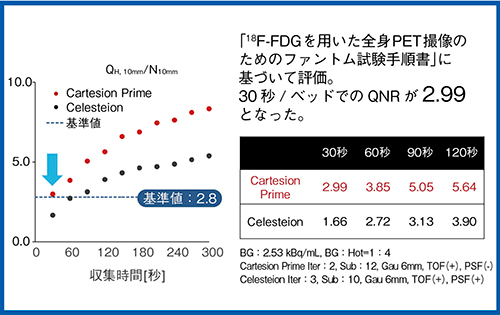
図3 ファントムを用いた画質評価
(データご提供:群馬県立県民健康科学大学・大﨑洋充先生)
症例3は悪性リンパ腫である。治療前にCelesteion,治療後にCartesion Primeで撮像し,病変部の集積の消失が確認された(図4)。Cartesion Prime(図4b,d)では,TOF効果による空間分解能の向上により,血液プールや縦隔および肝臓の集積が明瞭となり,ノイズも低減している。悪性リンパ腫の治療効果判定では,比較の基準となる縦隔や肝臓の集積が明瞭であることは,より正しい判定を行うために重要である。
また,小さな集積が明瞭に描出されることで,部分容積効果の影響が抑制され,定量性の向上にもつながる。
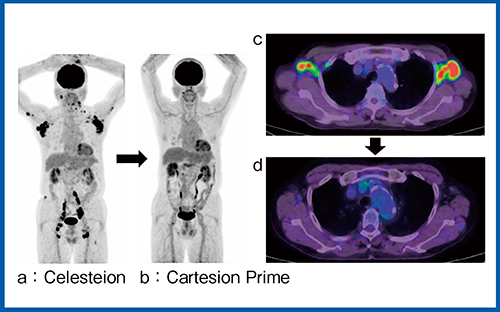
図4 Cartesion Primeによる治療効果判定
(症例3:悪性リンパ腫)
症例4(図5)は肺がんの骨転移(←)であるが,従来装置と比較して,Cartesion PrimeではSUVが上昇している。集積が明瞭となることで,より正しいSUVの測定が可能となる。
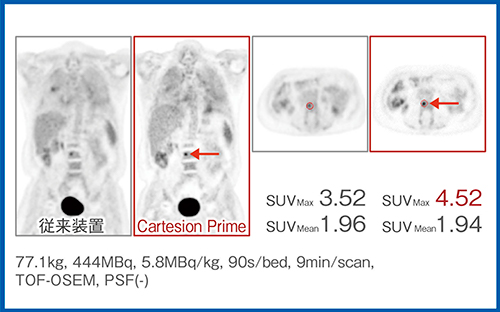
図5 Cartesion Primeによる小集積の定量性向上
(症例4:肺がん骨転移)
症例5(図6)は,右肺がんの放射線治療後で,腫瘍マーカーの上昇が認められた。診断用CTでは,放射線肺臓炎のため再発病変の特定が困難であったが,Cartesion Primeでは集積の強い再発病変(図6↓)と対側肺の新病変が指摘できた。
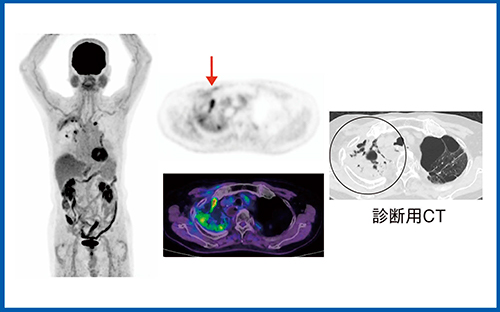
図6 Cartesion Primeによる再発の評価
(症例5:右肺がん放射線治療後)
症例6は,小児のウィルムス腫瘍の治療後である。診断用CTにて多発リンパ節腫大が指摘されたが,Cartesion Primeではそれらのうち,傍大動脈域にのみ集積を認め,バイアブルと判断された(図7)。
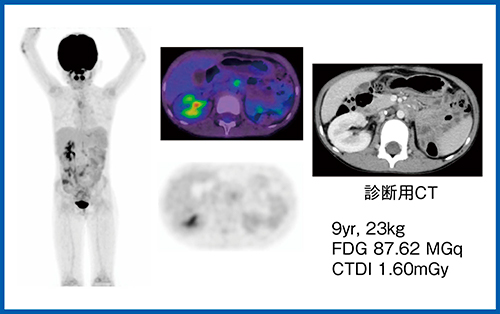
図7 Cartesion Primeによる転移再発評価
(症例6:小児のウィルムス腫瘍治療後)
デジタルPET/CTの将来展望:DLRによる画像再構成
デジタルPETでは,検出器の感度向上に加えて深層学習の技術を用いた画像再構成(Deep Learning Reconstruction:DLR)を行うことで,さらなる画質改善が期待されている。
症例7(図8)は,右副乳がん多発転移であるが,従来の画像再構成法(b)と比較し,DLR(c)では肺転移および肝転移への集積が明瞭化している。
自験例での検討では,DLRを適用することで明確な画質向上が認められたことから,将来的にはDLRが主流になるものと思われる。
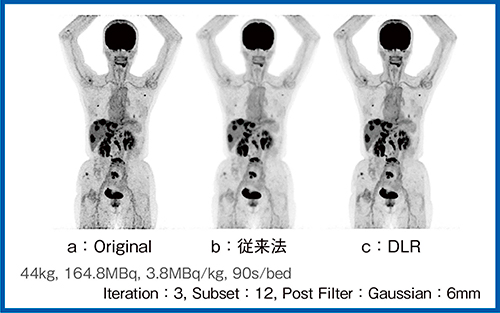
図8 DLR画像再構成の効果(W.I.P.)
(症例7:右副乳がん多発転移)
●参考文献
1)Lecomte, R. : Novel Detector Technology for Clinical PET. Eur. J. Nucl. Med. Mol. Imaging, 36(Suppl. 1):S69-85, 2009.
立石 宇貴秀(Tateishi Ukihide)
2014年〜東京医科歯科大学大学院医歯学総合研究科画像診断・核医学分野教授,横浜市立大学医学部放射線科客員教授。2015年〜順天堂大学医学部放射線科客員教授,東京工業大学非常勤講師,文京学院大学非常勤講師。2017年〜北海道大学大学院医学研究科病態情報学講座核医学分野客員教授。2019年〜群馬県立県民健康科学大学非常勤講師。
- 【関連コンテンツ】
