セミナーレポート(キヤノンメディカルシステムズ)
2022年11月号
第45回日本呼吸器内視鏡学会学術集会ランチョンセミナー7 最新のイメージング技術による肺がん、びまん性肺疾患診断
CT技術の進歩と気管支画像
森谷 浩史(大原記念財団大原綜合病院 画像診断センター)

CT開発の歴史を振り返ると、1990年代にヘリカルスキャンと高速化が実現し、ダイナミック撮影や三次元画像が一般臨床に普及した。また、1999年にマルチスライスCTが登場し、高速撮影による広範囲撮影が普及したことで、胸部診断へのCTの活用が可能になった。本講演では、キヤノンメディカルシステムズの高精細CTの技術的な特長を概説した上で、気管支の描出における有用性を報告する。
高精細CTにおける空間分解能の向上
CT装置の空間分解能を向上させる要素として、(1) 検出器画素サイズの小型化、(2) X線管球の小焦点化、(3) 線量を補うためのコンピュータ技術、(4) 撮影系統のブレの抑制や架台の補強、(5) コンピュータ再構成技術の進歩、などが挙げられる。キヤノンメディカルシステムズの高精細CT「Aquilion Precision」は、これらの実現によってきわめて微細な構造の描出を可能としている。
Aquilion Precisionでは、検出器画素サイズが従来CTの1/4となったことで空間分解能が従来CTの0.35mmから0.15mmに向上し、マトリックスサイズも従来CTの512×512マトリックスに対し、高精細CTでは1024×1024マトリックスの非常に微細な画像の取得が可能となった(図1)。
高精細CTに関する最初の臨床論文では、16列や64列の従来CTと比較して、肺野の既存構造や病変の性状が良好に描出されることが示された1)。実際に、高精細CTによる肺野の画像では既存構造の輪郭が非常に鮮明であり、日常臨床においてもきわめて精密な画像の提供が可能である(図2)。また、図3は同一症例における異なる焦点サイズの画像であるが、高精細CTの最小の焦点サイズ(0.4×0.5mm:b)では、従来CT相当の小焦点サイズ(0.6×1.3mm:a)の画像と比較し、気管支がより微細に描出されている。
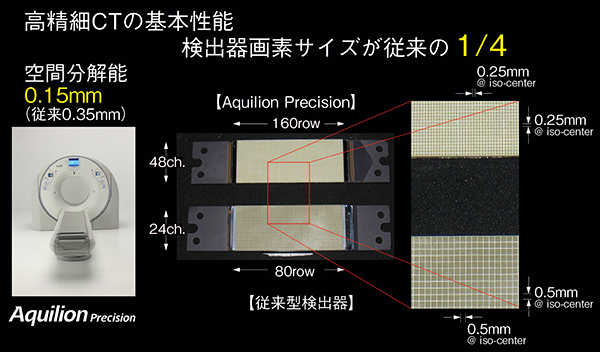
図1 高精細CTの基本性能
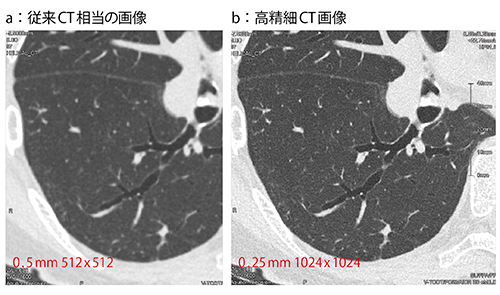
図2 従来CT相当と高精細CT画像の比較
高精細CT(b)では、肺野の既存構造の輪郭が明瞭であり、血管はより白く、気管支はより黒く描出されている。
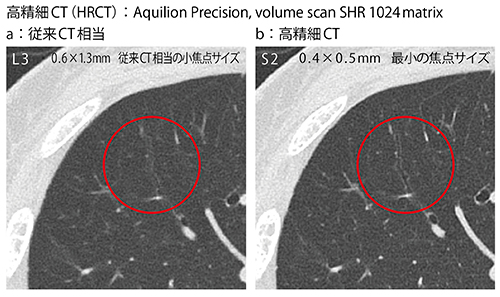
図3 従来CT相当と高精細CTにおける焦点サイズと画像の比較
図4は、CTを用いた死亡時画像診断(Ai-CT)の一例である。Ai-CTでは被ばく低減を考慮する必要がないため、高画質画像を目標とした撮影条件設定が可能である。図4では、1秒/回転という非常に高線量での撮影を行っており、肺野内の小葉や細葉の構造が明瞭に描出されている。われわれの検討では、高精細CTを用いたAi-CT画像にて、内径0.4mmの細気管支の描出が可能であった2)。
一方、臨床においては線量の増大に限界があるが、それを補うのがコンピュータ技術である。キヤノンメディカルシステムズ最新のディープラーニングを用いた画像再構成技術“Advanced intelligent Clear-IQ Engine(AiCE)”を用いることで、胸部単純X線写真と同程度の低線量でのCT撮影においても、従来の再構成法と比較してノイズが大幅に低減され、構造の適正な描出が可能となる(図5)。われわれの検討では、AiCEを用いることで、15mm径程度の肺結節を有する約90%の症例で関与気管支を描出でき、末梢病巣への気管支ルートを精緻に描出可能であった3)。
また、高精細CTのデータを用いた三次元画像解析も非常に進歩している。図6は、ザイオソフト社の三次元画像処理ワークステーション「Ziostation2」のMPR機能や血管計測機能を用いた気管支計測の一例である。関与気管支を非常に簡便に計測でき、超音波気管支鏡(EBUS)と同様に病巣と関与気管支の位置関係や病巣内気管支の有無などが確認できる。curved MPRやstraight viewなどを用いれば、CT画像上の病巣と関与気管支との位置関係をよりわかりやすく表示可能である(図7)。さらに、末梢結節の関与気管支については、葉気管支、区域気管支の入口部から次の分岐までの距離や分岐の角度、気管支径などがCT画像上で計測可能である4)。われわれは、CT画像上での気管支計測の結果から、通常鉗子による病変組織の採取の可能性や困難性などの予測について検討した。その結果、区域気管支の入口部から目標病巣までの距離が及ぼす影響は小さかったが、入口部から目標病変までの分岐が少ないほど到達が容易であった。気管支内径が大きいほど到達しやすく、また、目標病巣に至るまでの気管支主軸に対して角度が大きい分岐が存在する場合は、挿入が困難であることなどが推定された。
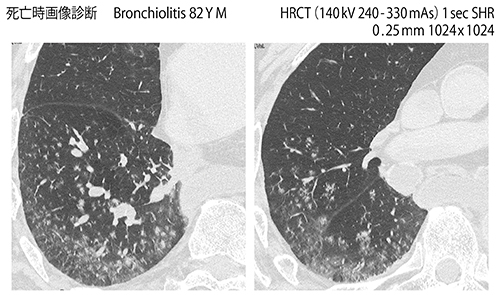
図4 CTを用いた死亡時画像診断の一例(82歳、男性)
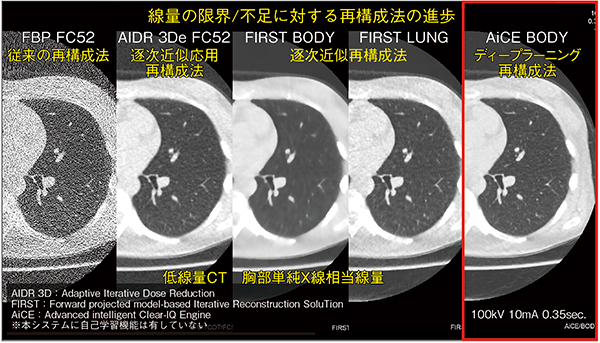
図5 線量の限界/不足に対する再構成法の進歩とディープラーニングを用いた画像再構成の有用性
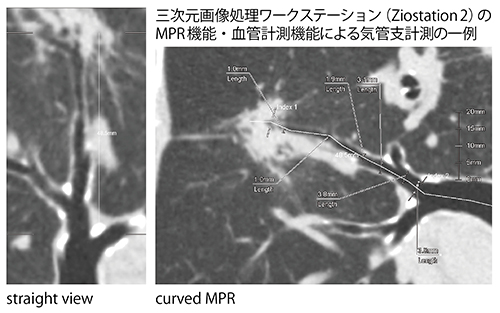
図6 三次元画像処理ワークステーションのMPR機能・血管計測機能による
気管支計測の一例
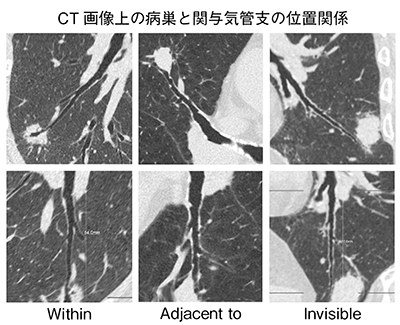
図7 CT画像上の病巣と関与気管支の位置関係
四次元動態CTを活用した動態・機能的データの取得
320列面検出器CT(ADCT)「Aquilion ONE」は、160mm範囲の連続撮影が可能である。4Dアプリケーションソフトウエア“4D Airway Analysis”を用いた1呼吸下で撮影したCT画像の解析では、呼吸に伴う気管支形状の変化を確認できる(図8)。現在は、連続呼吸下での2回のWide Volume Scanにより31cmの範囲の撮影が可能となり、肺全体や肺葉ごとの体積変動を計測できるほか、肺容積の経時変化が確認できるため、flow-volume曲線(FVC)の算出が可能である(図9)。図10は右下葉の入口部に閉塞がある症例であるが、右肺および上葉、下葉のみのFVCをそれぞれ描出している。現在、呼吸動態データと全肺気量(TLC)や機能的残気量(FRC)、最大吸気量(IC)などの呼吸機能との相関について検討を行っている。
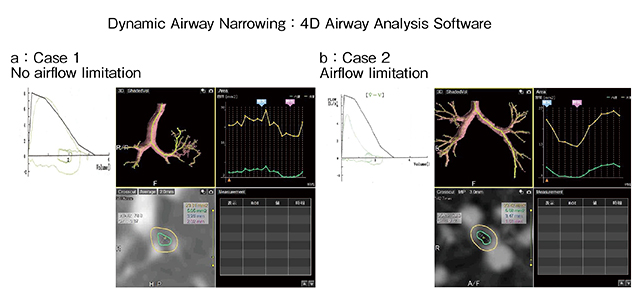
図8 4D Airway Analysisを用いた解析
case1(a)では呼吸による気管支形状の変化はほぼ見られないが、case2(b)では呼吸に伴い気管支形状が明らかに狭小化している。
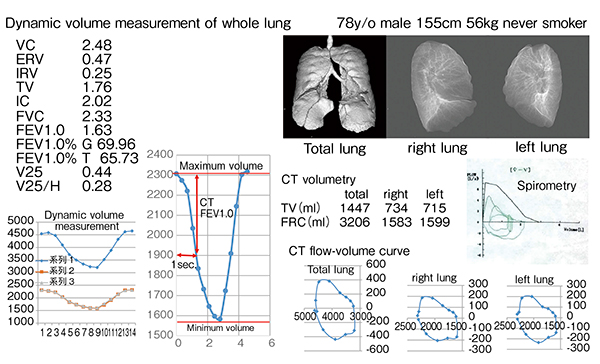
図9 健常例全肺のダイナミックボリューム測定(78歳、男性)
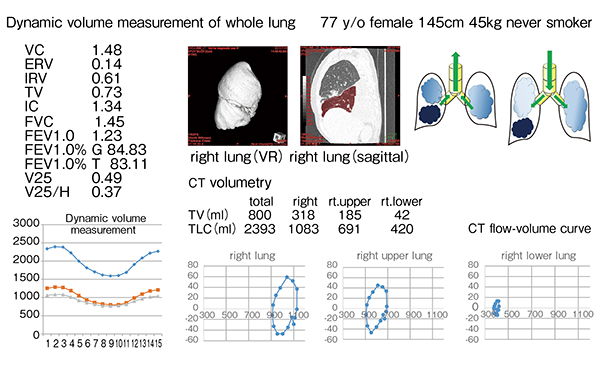
図10 右下葉の入口部に閉塞がある症例の全肺のダイナミックボリューム測定(77歳、女性)
ワークステーションを用いた三次元データの活用
現在、CT画像上での肺葉分割は、ワークステーションを用いて自動で高精度かつ容易に行うことができる。例えば、肺がんの術前検討として、テリトリーマッピング法を用いて、気管支や肺動脈の分岐、肺血流を基に切除予定部分の領域分割を行い、目標の領域を選んで描出することも可能である(図11)。当院では肺葉切除術前後に、肺葉ごとの体積計測と呼吸機能の計測を行っている(図12)。さらに、造影CT画像を基に肺動脈や肺静脈、気管支を色分けし、小葉の構造を立体的に観察することも可能である。これらの技術を活用し、肺の全体像から病巣周辺の血管や気管支を観察する“バーチャル切り出し”なども行っている。
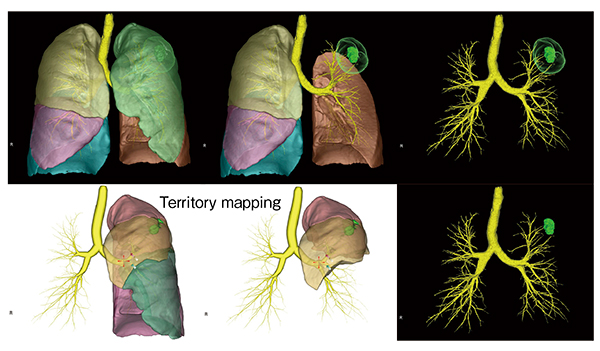
図11 テリトリーマッピング法を用いた肺の領域分割
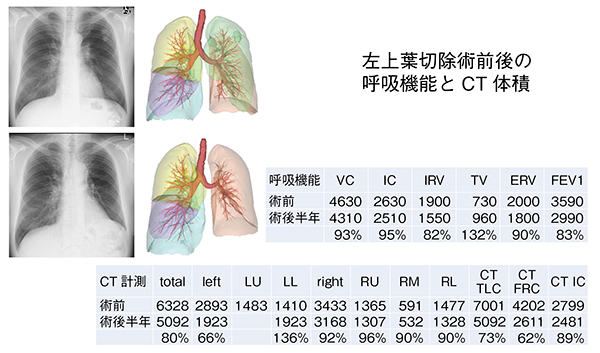
図12 左上葉切除前後の呼吸機能とCT体積
高精細CTによる吸気・呼気撮影
肺葉体積や気管支内腔は、吸気で拡張、呼気で縮小し、気管や肺野内の気管支の長さや形状が変動する。さらに、呼気時に気管支に屈曲が生じるケースもある。そのため、呼気と吸気の間の変化を示す動的な画像が得られれば、呼吸に伴う肺葉と気管支形態の変化の有用な解析が期待できる。
当院での肺葉切除後の症例を3例示す。症例1(図13)は右肺上葉切除後の症例であるが、吸気・呼気CTにて他肺葉の容積は変動するものの中葉(■)の容積は変動が少なかった。解析の結果、呼気時に中葉入口部が大きく屈曲し(図13 →)、特にB4の気管支が縦隔側に屈曲していることから、内腔の狭小化が生じていることが確認できた。
同様に、症例2(図14)も右肺上葉切除後の中葉の動きが悪く、吸気時には細気管支が多く描出されているが、呼気時は気管支内の容積が減少し、描出が不明瞭であった。中間気管支幹の屈曲が見られ(図14 →)、それが描出不良の要因であるかは定かではないものの、ほかの症例とは明らかに動きが異なっていた。
症例3(図15)は、右肺上葉部分切除後の症例で、中葉(■)の動きが悪かったものの、気管支はきれいに拡張・収縮し、気管支形態や開存は良好であった。画像解析の結果、本症例は胸膜播種が広範に広がり、中葉前面に播種による癒着が生じたことに由来することが推定された。
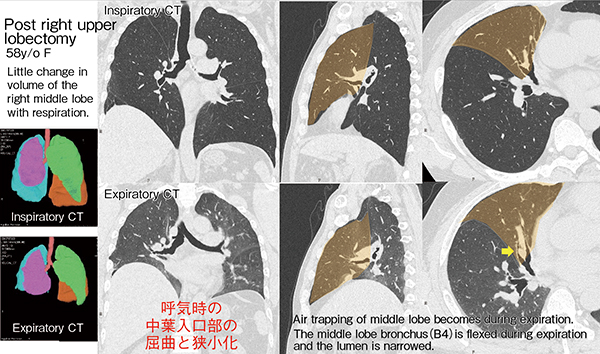
図13 症例1:右肺上葉切除後(58歳、女性)
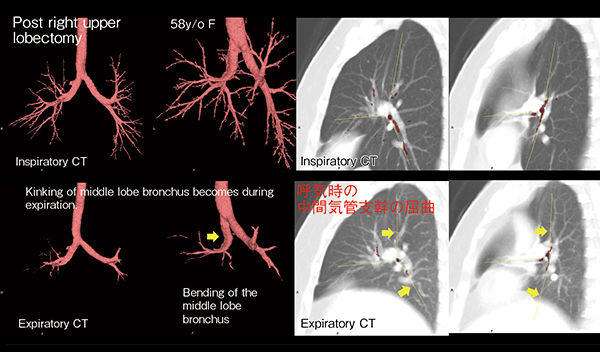
図14 症例2:右肺上葉切除後(58歳、女性)
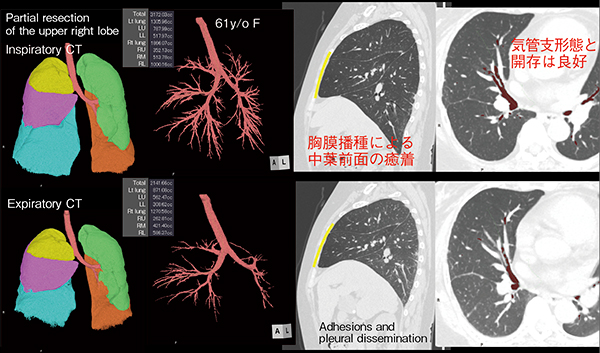
図15 症例3:右肺上葉部分切除後(61歳、女性)
まとめ
高精細CTは、気管支形態を精緻に描出・計測でき、内径0.4mmの小葉内細気管支の描出や末梢肺野病巣への気管支ルートの描出も可能である。四次元動態CTは呼吸動態、機能データ、動的立体データを取得することができる。さらに、吸気・呼気撮影により、呼吸に伴う肺葉と気管支形態の変化や機能を解析可能であり、今後、これらの技術のさらなる発展が期待される。
*記事内容はご経験や知見による、ご本人のご意見や感想が含まれる場合があります。
*AiCEは画像再構成処理の設計段階でAI技術を用いており、本システム自体に自己学習機能は有しておりません。
●参考文献
1)Kakinuma, R., Moriyama, N., Muramatsu, Y., et al. : Ultra-high-resolution computed tomography of the lung : Image quality of a prototype scanner. PLoS ONE, 10(9), 2015.
2)Moriya, H., et al. : Basic study of bronchial imaging of ultra-high-resolution CT using maximum exposure dose. RSNA 2019.
3)Moriya, H., Muramatsu, S., Chiba, H., et al. : Depiction of Reachable Bronchi of Peripheral Lung Nodule for TransbronchialApproach by Ultra-High Resolution CT (UHRCT). RSNA2019 VI131-ED-X after December 6, 2019.
4)肺結節に対する経気管支的生検のための気管支ルート選択技術の臨床的検討.第44回日本呼吸器内視鏡学会学術集会, 2021.
一般的名称:全身用X線CT診断装置
販売名:CTスキャナ Aquilion Precision TSX-304A
認証番号:228ACBZX00019000
一般的名称:全身用X線CT診断装置
販売名:東芝スキャナAquilion ONE TSX-301A
認証番号:219ACBZX00029000
- 【関連コンテンツ】
