PICK UP
BeamSat による選択的TOF MRAの開発
西原 崇(株式会社日立メディコMRIシステム本部ソフト開発部)
2013-9-25
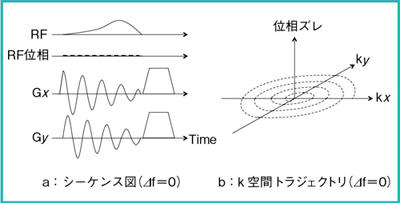
図1 BeamSatパルス(⊿f=0)
3D TOF(Time of Flight)は頭部血管の描出法として広く用いられているが,複雑な血行動態を描出することは困難である。そこで今回,ナビゲーターエコーなどに用いられているBeam型の励起パルス1)をプリサチュレーションパルスとして用いて特定血管の信号を抑制し(以下,BeamSatパルス),3D TOF MRAと併用することで,頭部の複雑な血行動態を非造影で描出する方法を検討した2)。本稿では,BeamSatパルスの基本性能と臨床適用例について紹介する。
励起プロファイルの安定性評価
Beam型の励起パルスには,静磁場不均一により励起プロファイルが歪みやすいという欠点がある。静磁場不均一が変化した場合の励起プロファイルを計算機シミュレーションで評価した。
BeamSatパルスの簡単なシーケンスを図1aに示し,その際のk空間トラジェクトリを図1bに示す。静磁場不均一⊿fは,RFの照射周波数と励起する局所の共振周波数のズレとなり,シーケンスとk空間トラジェクトリに対して図2に示すような影響を及ぼす。すなわち,k空間の中心に向かって,線形に位相のズレが大きくなる。⊿f(0〜150Hz)による励起プロファイルの変化のシミュレーション結果を図3に示す。⊿fにより励起プロファイルがブロードになることがわかる。なお,シミュレーション結果は単純化するために,kx方向のみを示している。
人体に対して内頸動脈(ICA)付近の静磁場不均一を計測したところ,最大で50Hz程度であった。目的をFA=90°,Beamの直径φ=30mmとした場合,上記シミュレーションの結果より,50Hzの強い不均一があった場合でも,FA=81°,φ=33mmの歪みに抑えることができる。
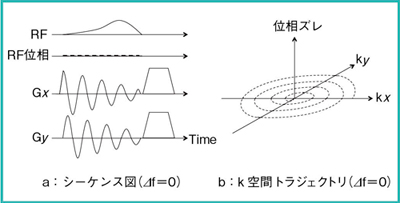
図1 BeamSatパルス(⊿f=0)
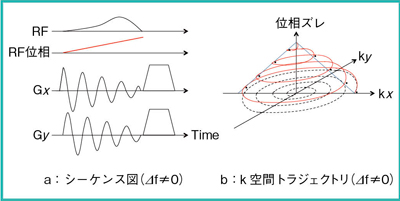
図2 BeamSatパルス(⊿f≠0)
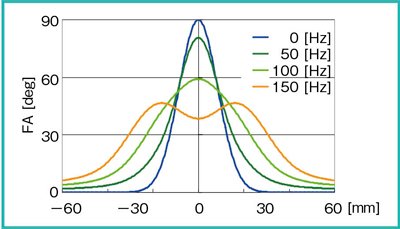
図3 励起プロファイルシミュレーション結果 (⊿f=0~150Hz)
BeamSatの設定位置
目的血管を選択的に抑制するためには,それ以外の血管を抑制しないようにBeamSatの設定位置が重要になる。健常ボランティアにおいて,片側のICAのみを選択的に抑制できるBeamSatの位置を検討した。検討の結果,サジタル断面では鼻根部とトルコ鞍に接する位置に設定し,アキシャル断面では錐体-斜台に接する位置に設定することで(図4),椎骨(VA)-脳底動脈(BA)や中大脳動脈(MCA)など,目的以外の血管の抑制を防げることがわかった。
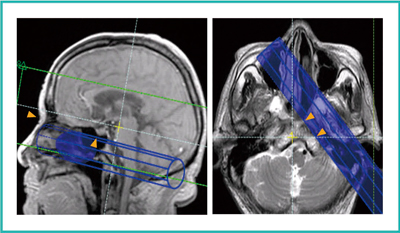
図4 BeamSatの設定(左ICA岩様部抑制)
SAG断面:鼻根部とトルコ鞍に接する位置
AX断面:錐体-斜台に接する位置
BeamSat専用UI:BeamSatの表示は,実線部分が位置決め画像より手前側,破線部分が奥側,ハッチング部分がBeamSatと位置決め画像の交面である。
抑制効果の評価
BeamSatパルスによる血流信号の抑制範囲と抑制率を調べた。BeamSatの位置は上記の基準で設定し,BeamSatパルスあり,なしの2回撮像した。使用装置は1.5T MRI(日立メディコ社製),受信コイルは8ch Head,3D TOFの撮像条件はTR/TE=46.2ms/6.9ms,撮像マトリックス512×224である。取得した素画像で,ICA〜MCA-M4の各位置で信号強度を計測した。計測した信号強度を表1に,撮像結果(MIP像)を図5に示す。BeamSatなし(通常のTOF)では末梢になるほど信号強度が低下しているが,BeamSatありでは末梢になるほど信号強度が上昇している。これは,ICAで抑制された磁化が,末梢に移動するに従ってT1緩和で信号が回復している様子を示していると考えられる。また,MCA-M4 になると,背景である脳実質よりも血液の信号値が大きくなっており,MIP画像においてMCA-M4がわずかに視認できることと一致している。
以上の結果より,血流速にも依存するがICAを抑制した場合,MCA-M3程度まで安定的に抑制できることがわかった。
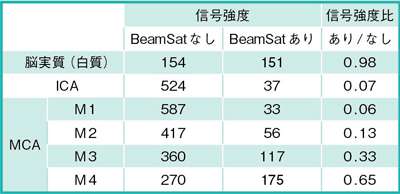
表1 ICA~MCA-M4の信号強度(健常例)
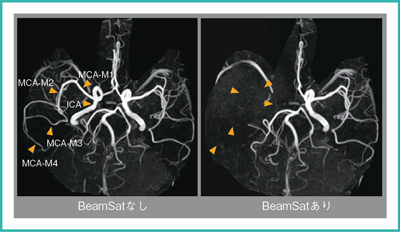
図5 BeamSat TOF画像(健常例)
BeamSatあり(右)では,ICAからMCA-M3は視認できない程度に抑制できているが,MCA-M4はわずかに視認できる。
また,左MCAと後大脳動脈が,BeamSatありとなしで描出能はほとんど変化していないことがわかる。
*本画像は,撮像目的・意義を説明し,文書による同意を得た健常人ボランティア画像である。
臨床適用例
本技術を臨床に適用した結果を3例示す。まず,右頸部内頸動脈狭窄症例への適用結果を図6に示す。図6aのCE-MRAの所見より,右頸部内頸動脈に狭窄が確認できる。図6b(1)に示した通常の3D TOF画像では,狭窄により血流が少ないものの,左右の脳内への血行は保たれているように見える。ここで,BeamSatパルスを右ICAに印加した図6b(2)において右MCAが描出されていること,および左ICAに印加した図6b(3)において右MCAが抑制されていることから,左ICAからAcomAを介して右MCAに血液が流入するcross flowのある症例であることがわかる。また,図6 b(2),(3)において,左右のPCAがともに抑制されていないことから,PcomAを介した前後のcross flowがほとんどないこともわかる。
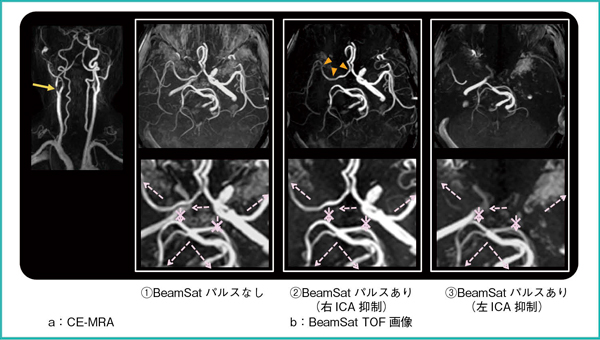
図6 臨床画像1:右頸部内頸動脈狭窄
a:右ICAに狭窄が確認できる(→)。
b(1):右側の血流が低下しているものの脳内への血行は保たれているように見える。
b(2),(3):右MCAは,左ICAからAcomAを介したcross flowにより養生されていること,およびPcomAを介した前後のcross flowがほとんどないことがわかる。
次に,左頸部内頸動脈狭窄症例への適用結果を図7に示す。図7 aの2D TOF-MRAの所見より,左頸部内頸動脈に狭窄が確認できる。図7 b(1)に示した通常の3D TOF画像では,左右の脳内への血行は保たれているように見える。ここで,BeamSatパルスを右ICAに印加した図7 b(2)において,右MCAとともに右PCAが抑制されていること,および左ICAに印加した図7 b(3)において,左MCAとともに左PCAが抑制されていることから,ICAからPcomAを介して,左右それぞれのPCAに血液が流入するcross flowがある症例であることがわかる。また,図7 b(2),(3)において,逆側のMCAが抑制されていないことから,AcomAを介した左右のcross flowがほとんどないこともわかる。
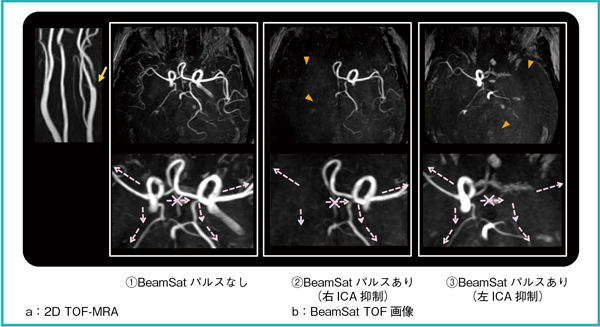
図7 臨床画像2:左頸部内頸動脈狭窄
a:左ICAに狭窄が確認できる(←)。
b(1):脳内への血行は保たれているように見える。
b(2),(3):左右のPCAは,それぞれ左右のICAからPcomAを介したcross flowにより養生されていること,およびAcomAを介した左右のcross flowがほとんどないことがわかる。
最後に,左浅側頭動脈(STA)-MCAバイパス術の術後評価に適用した結果を図8に示す。図8 aに示した通常の3D TOF画像で左MCA領域に血流信号が確認できるが,バイパスを介した血流が描出されているのか,左ICAからの血流が描出されているのかの詳細な血行動態は判断が難しい。ここで,BeamSatパルスを左STAに印加した図8 bにおいて,左MCA領域が抑制されていることから,左MCAはSTAからバイパスを介した血流であることが確認できる。
以上に示した結果より,ウィリス輪やバイパスを介した頭部の複雑な血行動態を描出可能であることがわかった。
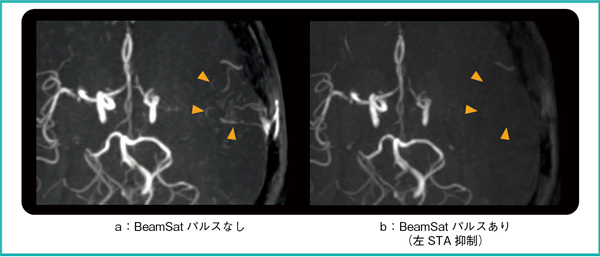
図8 臨床画像3:左STA-MCAバイパス手術後
a:左MCA領域の血流信号が確認できる(▶)。
b:左MCAが抑制されており,左MCAは左STAからバイパスを介した血流であることが確認できる。
まとめ
本稿では,BeamSatパルスの基本性能と臨床適用例について紹介した。今後は,TOF以外のさまざまな非造影MRAに適用し,全身の血行動態の把握に役立てていきたい。
●参考文献
1)Pauly, J., et al. : IEEE. Trans. Med. Imaging, 10, 53〜65, 1991.
2)Nishihara, T., et al. : Selective TOF MRA using BeamSaturation pulse, Proc. ISMRM 2012, 3698.
