NAEOTOM Symposium 2025
2026年4月号
NAEOTOM Alphaの臨床アドバンテージ
腹部領域 NAEOTOM Alphaによる新たな臨床価値の創造
横山 幸太(東京科学大学病院放射線診断科)

本講演では,当院での経験を基に,腹部領域におけるフォトンカウンティングCT(PCD-CT)「NAEOTOM Alpha」の実臨床での有用性,機器の価格に見合う価値,機器導入のモチベーションになる活用法の観点から,肝胆膵領域および消化管領域におけるSpectral Imagingについて報告する。
肝胆膵領域における有用性
1.低keVによる造影効果増強
Spectral Imagingは,物質固有のX線吸収係数の差を利用して物質弁別する手法である。ヨード造影剤はK吸収端が約33.2keVにあり,低keVにするほど既存組織との差が大きくなるため,造影効果を増強することができる。実臨床では,これを病変の視認性向上に活用できる。
乏血性腫瘤である膵がんでは,低keVにすることで正常膵の造影効果が強調され,病変のコントラストが向上し,視認性が向上する。図1は膵尾部がんであるが,NAEOTOM Alphaの低keV画像(図1 b)では視認性が向上し,特に40keVでは正常膵との境界がより明瞭である(←)。
低keVの有用性は以前から知られているが,dual energy CTではノイズ増加が課題となっていた。これに対してNAEOTOM Alphaでは,40keVでも診断に影響ないレベルにノイズが抑制され,病変の視認性が大幅に向上することから,演者は40keVを実臨床で用いている。
NAEOTOM Alphaでは,読影支援システム「syngo.via」を用いて低keV画像を容易に作成できる。撮影前にプロトコール設定が必要なdual energy CTと異なり,後方視的に任意のkeVに変更できる点は非常に大きなメリットである。なお,ノイズや造影効果は線量や造影剤量によっても変化するため,例えば病変の視認性重視では40keVが優れるが,被ばく低減のため低線量撮影や肥満体型でノイズが多くなる場合などは,50〜55keVにするなど症例に応じて至適keVを調整するとよい1)2)。
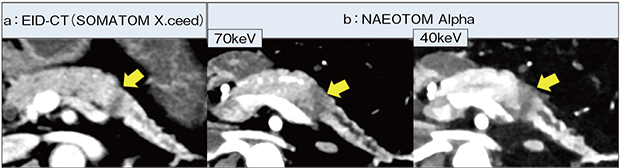
図1 NAEOTOM Alphaによる膵尾部がんにおける低keV画像の評価
2.見えなかったものが見える
膵がんにおいては,従来のdynamic CTも高い診断能を有しているが,NAEOTOM Alphaには「今まで見えなかったものが見える(See the Unseen)」という,高額機器導入に見合った価値がある。
膵がんの診断では,動脈相で正常膵とのコントラストを見ることが一般的であり,平衡相ではがんを認識しづらい(図2 a←)。これに対して,NAEOTOM Alphaの40keV画像では,平衡相における遅延性増強(線維化)が明瞭化する(図2 b←)。膵がんを目的としたdynamic CTにかぎらず,救急や他のがんのフォローなど別目的で撮影された平衡相の造影CTでも膵がんの評価が可能なことは,NAEOTOM Alphaの大きな価値と言える。
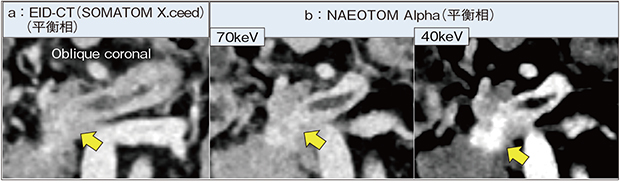
図2 NAEOTOM Alphaの低keV画像による平衡相での膵がんの描出
3.造影剤量低減
NAEOTOM Alphaは造影剤減量効果も大きい。図3は,がんフォローのため複数回撮影されている症例である。従来,EID方式のDual Source CT最上位機種である「SOMATOM Force」では,通常量(体重比2倍)に相当する80mLの造影剤で撮影されていたが,腎機能低下を認めたため,NAEOTOM Alphaでは造影剤を半量の40mLに減量して撮影を行った。40keV画像では,造影剤量を半減したにもかかわらず,肺動脈末梢および主膵管の描出はむしろ向上している(図3 b↑)。急性腎障害のリスクを有する症例では,eGFR×2~3倍の造影剤量が安全域とされており,30~40mL程度であればeGFR 15前後の患者においても,造影検査を安全に施行できる可能性が示唆される。
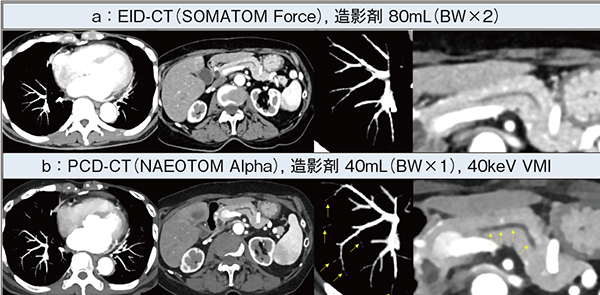
図3 低keVによる造影剤減量効果
消化管領域における有用性
1.定量評価と病理対比
消化管領域では,クローン病におけるNAEOTOM Alphaのエビデンスが報告されている。図4は実際の症例で,再発時にNAEOTOM Alphaで撮影したところ,低keVにすることで活動性病変の視認性が向上した(図4 a,b ↑)。また,dual energy CTとPCD-CTに関する研究でヨード値が炎症の活動性と相関があることが示されており3),4),ヨード値による急性炎症の定量が実臨床において有用である(図4 c)。さらに,40keV画像では肛門皮膚瘻など副所見の描出能も向上し,治療介入判断にも大きく寄与する。一度の撮影で,消化管とそれ以外の包括的評価が可能になることも非常に大きなメリットである。
消化器がんにおいては,NAEOTOM Alphaの低keV画像によりT因子を評価できる可能性がある。図5は,MRIのT2WIで筋層の断裂が確認され,漿膜下浸潤が疑われた直腸がん症例で,NAEOTOM Alphaの低keV画像でも壁の断裂や漿膜下に突出する病変の様子を認識できた(↑)。病理学的にも漿膜下浸潤が確認されcT3と診断されており,CTでT因子を詳細に評価できる可能性があると考え,当院で検討を進めている。
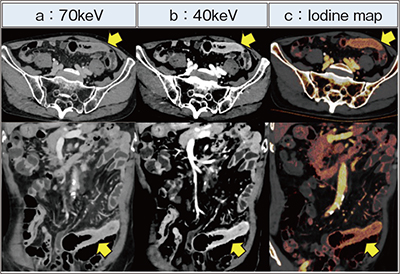
図4 NAEOTOM Alphaによるクローン病の活動性病変の評価
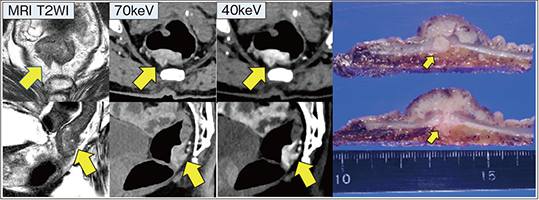
図5 NAEOTOM Alphaによる直腸がんの漿膜下浸潤の評
2.さらなる展望
低keV画像は治療効果の評価にも活用できる可能性がある。直腸に全周性の病変が認められ,術前化学療法を行った進行直腸がん症例(図6)についてNAEOTOM Alphaで撮影したところ,特に40keV画像やヨードマップでは一部に造影効果が残っており(↑),FDG-PET/CTでも同部位に集積が認められた。Spectral Imagingでは化学療法後の残存病変の検出がより鋭敏になると考えられ,治療効果判定への応用が期待される。
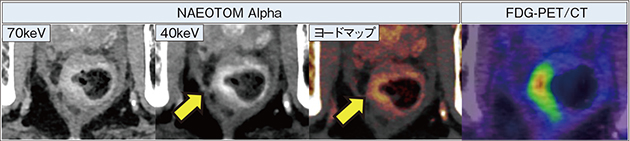
図6 NAEOTOM Alphaによる化学療法後の残存病変の検出
3.syngo.viaを使いこなす
当院では,富士フイルム社製PACS端末にsyngo.viaを相乗りして利用している。ビューワ画面上のsyngo.viaボタンをクリックすると,AIによる画像認識で適切なアプリケーションが自動で立ち上がり,スムーズにSpectral Imaging解析を行える。任意のkeVに設定できる「Monoenergetic Plus」や造影CT 1相から仮想単純画像を作成する「VNC」,ヨードを定量化する「Iodine map」,VNCとヨードマップの重ね合わせ画像などを簡単に作成できる。
まとめ
NAEOTOM Alphaは膵がんや消化器がんにおいて実臨床で大きなメリットがあり,見えなかったものが見えるSee the Unseenを超え,見ようとさえしなかったものを見ることができるBeyond the Unseenを可能にする。特に消化器内科,肝胆膵外科,腎臓内科への訴求効果が高く,患者にとっても被ばく低減や撮影回数の減少などメリットが大きい。「膵がんが見やすくなる」「慢性腎不全でも安全に造影検査を行える」「術前検査,術後検査を1回で完了できる」といった実臨床における有用性は,機器導入のモチベーションとなりうるものである。Spectral Imagingは,Single Source CT「NAEOTOM Alpha.Prime」でも可能であり,NAEOTOM Alphaが新たな標準として医療現場に普及することを期待したい。
●参考文献
1)Willemink, M., et al., Radiology, 289(2): 293-312, 2018.
2)Esquivel, A., et al., Korean J. Radiol., 23(9): 854-865, 2022.
3)Dane, B., et al., Radiology, 301(1): 144-151, 2021.
4)Dane, B., et al., Abdom. Radiol. (NY), 49(1):271-278, 2024.
横山 幸太(Yokoyama Kota)
2012年 金沢大学医学部卒業。国立精神神経医療研究センター,国立国際医療研究センターなどを経て,2019年 東京医科歯科大学(現・東京科学大学)放射線科特任助教。2020年 同助教。2023年〜同講師。
