セミナーレポート(キヤノンメディカルシステムズ)
日本超音波医学会第91回学術集会が,2018年6月8日(金)〜10日(日)の3日間,神戸国際会議場(兵庫県神戸市)などを会場に開催された。10日行われたキヤノンメディカルシステムズ株式会社共催ランチョンセミナー14では,和歌山県立医科大学循環器内科の赤阪隆史氏が座長を務め,聖マリアンナ医科大学循環器内科の出雲昌樹氏と東住吉森本病院循環器内科の宮崎知奈美氏が,「キヤノンメディカルシステムズが提供する心エコー装置の新たな展開2018」をテーマに講演を行った。
2018年10月号
日本超音波医学会第91回学術集会ランチョンセミナー14 キヤノンメディカルシステムズが提供する心エコー装置の新たな展開2018
Aplio i-Seriesで診る心臓の機能 〜虚血に迫る〜
宮崎知奈美(東住吉森本病院循環器内科)
東住吉森本病院は,大阪市東住吉区にある329床の民間病院である。本講演では,市中病院の日常臨床で最も相対することの多い虚血性心疾患について,キヤノンメディカルシステムズの超音波診断装置「Aplio i900」による冠動脈血流速度測定,“Wall Motion Tracking”(2D/3D)によるストレイン解析を中心に述べる。
経胸壁3Dセクタプローブによる心臓の描出
Aplio i-seriesの最高機種であるAplio i900では,Volume Matrixプローブとして3D-TEE(経食道)プローブと経胸壁セクタ3Dプローブを搭載している。新しい経胸壁3Dセクタプローブは,2D用のプローブとほぼ同じ大きさで,軽量でケーブルが柔らかくなり,取り回しが容易になった。また,画角も従来機種の90°から最大120°に広がり,拡大心でも心尖部を含めて心臓全体をカバーすることが可能になった。
しかし,3Dデータ収集やストレイン計測が可能になったと言っても,超音波の基本はBモード画像である。Aplio i900では,Bモード画像の画質が大きく向上しており,心筋内の微細な構造までクリアに観察できる。特にニアフィールドは,従来はアーチファクトによって霧がかかったような画像だったが,Aplio i900では繊細かつクリアな画像が得られている。また,カラードプラについても解像度が向上している。
これらは,Aplio i-seriesの“iBeam Forming”と呼ばれる技術で,送受信するビームを細く均一にすることで可能となった。その効果は,日常診療でよく遭遇する肥満体型など,描出が困難な患者の検査で実感する。図1は,ICUにて気管内挿管中の患者で左側臥位の体勢が取れず,臥位で記録した画像である。従来装置の画像では,心臓の動きはわかるが詳細な形態までは確認できない。Aplio i900でも,臥位のため肺がかぶっており決して画像は良好とは言えないが,診断可能な情報は得られている。これは超音波による心臓検査でも最もタフなケースと言えるが,それでも診断が可能な画像が得られていることは特筆すべきことである。
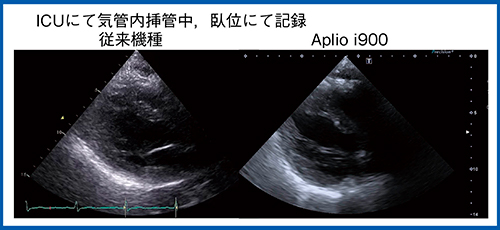
図1 画像不良症例でのside by side比較
冠動脈血流予備能の測定
2018年度の診療報酬改定において,安定労作性狭心症へのインターベンション(PCI)について,90%以上の狭窄か,明らかに狭窄が原因と考えられる症状がある場合,および機能的虚血評価の検査により虚血の原因と確認されている狭窄のみ算定できることとなった。
心筋虚血の進行は,心筋の灌流異常から始まり,代謝異常,拡張能異常,収縮能異常,ECG変化に至る虚血カスケードで説明される。それぞれのステージで,さまざまな機能的虚血の評価方法があるが,灌流異常はカテーテル検査中にプレッシャーワイヤで計測する部分冠血流予備量比(FFR)が一般的に用いられている。冠血流量については,経胸壁心エコーによる冠動脈血流予備能(CFR)の計測で同様の評価が可能であり,運動負荷やドブタミン負荷エコーと併せた評価が可能になることから,心エコーを用いた虚血の機能的評価は,今後,重要性が増すものと考えられる。
1.経胸壁心エコーによるCFRの計測
経胸壁心エコーによるCFRは,冠動脈に対して安静時とATP負荷後の拡張期平均血流速度を測定し,その比を取って求める。ATP(140mg/kg/min)負荷,約1分後には,反応性充血によって血流が増加する。基本的に前後の比が2倍以上で正常,2倍以下であれば虚血があると考えられる。経胸壁心エコーによる左前下行枝(LAD)の描出では,右室と左室の間の前室間溝をターゲットにプローブを当てて,拡張期の赤いドプラ信号を探す。これがLADの血流で,正常であれば拡張期優位の血流速度波形となり,収縮期には遅く拡張期には速い波形を得ることができる。一方で,LADに比べて,右冠動脈(RCA)や左回旋枝(LCX)の描出は難易度が高い。しかし,Aplio i900では描出能が向上しており,従来よりRCAやLCXの描出がしやすくなり,血流速度の検出能も向上している。
2.日常臨床におけるCFRの活用法
症例1は,75歳,男性,右冠動脈近位部にステント留置後に症状を訴え,冠動脈CTを施行した。LADとRCAに中等度の狭窄を認め,特にLADは石灰化が強く,CTAでは内腔の評価は困難だった。CTは,冠動脈評価に有効なモダリティだが,石灰化がある場合には狭窄の評価が難しくなる。そこで,エコーによるCFRをLADとRCAで測定した(図2)。LADは安静時に比べて,ATP負荷時には血流速度が約3倍に増加している。また,RCAはウォールモーションなどのノイズが入りLADほどきれいには測定できていないが,血流速度は負荷時には安静時の3倍に増えていることから,LAD,RCA共に有意な狭窄ではないと考えられた。
経胸壁心エコーを用いたCFRについて,LADで狭窄・虚血の診断能を検討した文献では,冠動脈造影,運動負荷心筋シンチグラフィに対して,感度と特異度でいずれも8割から9割の高い診断能があることが報告されている1)〜3)。CFRは,血流がしっかりととらえられる症例では,日常臨床で使える検査方法だと言える。
また,日常診療では,薬物負荷をしてCFRを求めなくても,安静時の血流速度そのものが診断に役立つこともある。症例2は92歳女性,呼吸困難がある患者で,心不全を疑い超音波検査を施行した(図3)。心エコー(図3 a)では,心尖部は広範に無収縮(akinesis)であり,一方,心基部は過収縮で対称性の動きが認められ,たこつぼ型心筋症が疑われた。心電図(図3 b)では前胸部誘導でSTの上昇が見られることから,LAD領域の急性心筋梗塞の可能性も考えられた。カラードプラでは血流速度は速いが,拡張期優位の順行性の血流がLADに認められることから,少なくとも完全閉塞は否定的であり,緊急の冠動脈造影は必要ないと考えられた(図4)。後日行った冠動脈造影でも,狭窄は認められずスパスムの誘発もなかったことから,たこつぼ型心筋症と診断できた。
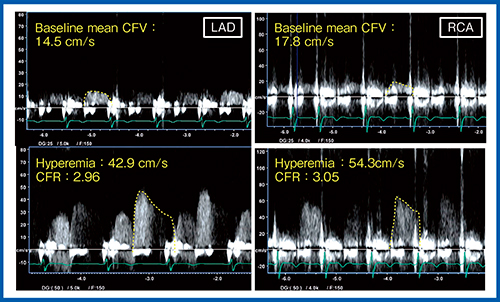
図2 症例1(右冠動脈近位部にステント留置後)の冠動脈血流予備能(CFR)
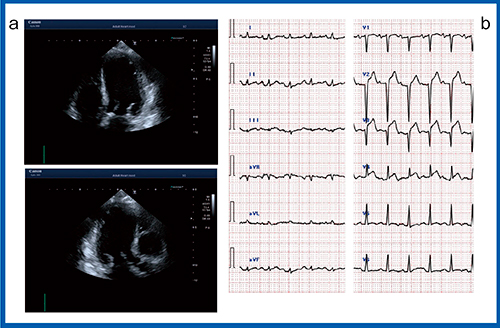
図3 症例2:たこつぼ型心筋症疑い
a:心エコー b:心電図
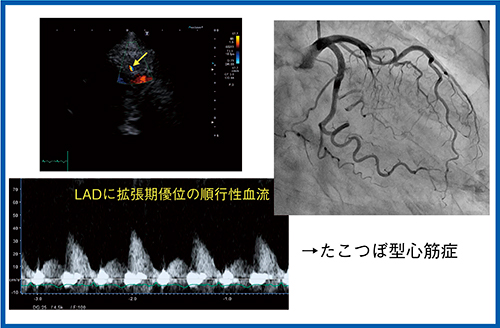
図4 症例2のLADの冠動脈血流予備能
Wall Motion Tracking(WMT)によるストレイン解析
次に,Aplio i900の壁運動解析アプリケーション(2D/3D-WMT,global longitudinal strain)を用いた心筋のストレイン解析について述べる。心筋のストレイン解析は,局所壁運動異常(安静時,負荷時)の客観的な指標となり,心筋バイアビリティの評価なども可能である。
1.2D-WMT
安静時の局所壁運動異常の症例を示す。症例3はHFrEF(heart failure with reduced EF)で,全体的に心臓の動きが低下しており,局所の壁運動の低下部位を指摘することは難しい(図5)。そこで,2D-WMTによるストレイン解析を行ったところ,長軸方向のlongitudinal strainで側壁のmid領域に低下が認められた(図6)。ブルズアイではほかに,前壁(anterior)や後側壁(inferolateral)が低下していることがわかり,自由壁側を中心に異常が確認できた(図6 右下)。冠動脈造影では,LADの狭窄のほかに,LCXの#12が完全閉塞(CTO)となっており,PCIが施行された。HFrEFで,全体の機能低下か,局所の壁運動異常か判断に迷う場合に,ストレインによる解析が有効だと思われる。
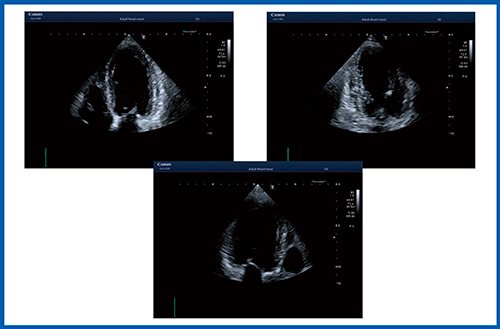
図5 症例3:HFrEF(機能低下は全体的か,局所的か?)
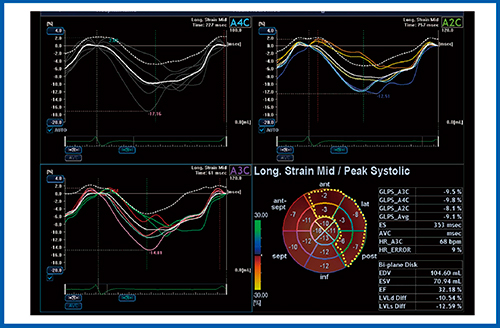
図6 症例3のlongitudinal strain
しかし,安静時の検査で虚血が診断できるものは限られており,負荷をかけた検査が基本となる。症例4は,77歳,男性,労作時の胸部圧迫感があり,トレッドミルの運動負荷による超音波検査を施行した。2 chamber view(図7)のbaseline(a),peak stress(b),recovery(c)の画像では,peak stressで心尖部前壁側の運動低下が認められた。さらに2D-WMTを行ったところ,運動負荷前後のlongitudinal strainをポーラーマップで表示すると,peak stressでほかの部位の動きに比べて心尖部前壁の動きが落ちていることが確認できた(図8)。この症例では,心拍数が90前後で胸痛が発生し,さらに負荷をかけることができず,systolic strainの値でpeak stressを計測し虚血を判断できた。しかし,通常はストレスをかけ続けるとストレインはどこかで頭打ちとなり,ストレインの値だけでは虚血の判断が難しく,post-systolic shortening(PSS)やdiastolic stunningなどを併せて判断することが必要となる。
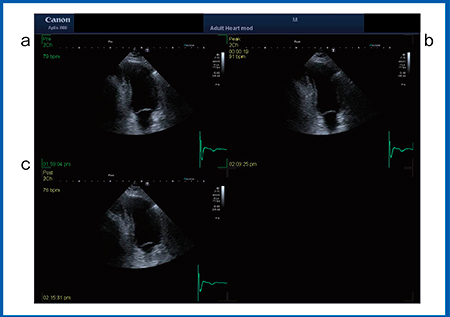
図7 症例4の2 chamber view
a:baseline b:peak stress c:recovery
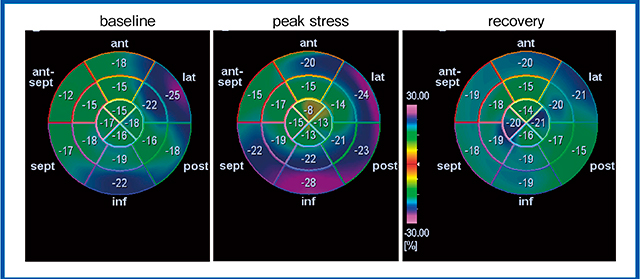
図8 症例4の運動負荷後のlongitudinal strainの変化
2.3D-WMT
Aplio i900では,2D-WMTに加えてボリュームデータを基に評価する3D-WMTが可能になっている。3D-WMTでは,心筋のスペックルを三次元的にトラッキングすることで,より正確な壁運動解析が可能になる。3D-WMTでは多くの指標が得られるが,なかでも心筋の面積の変化率を示すArea Change Ratio(ACR)が,longitudinal strainとcircumferential strainと比較して心筋の収縮能を最も良く反映することが報告されている4)。
図9は,前壁中隔に梗塞が認められる急性心筋梗塞(a)とたこつぼ型心筋症(b)の3D-WMTによるストレイン解析である。3D-WMTではストレイン低下の空間的な広がりを瞬時に把握でき,直感的に理解できるのがメリットである。
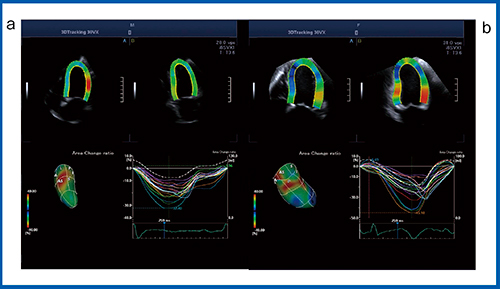
図9 3D-WMTによるストレイン解析
a:急性心筋梗塞 b:たこつぼ型心筋症
3.Global longitudinal strain(GLS)
ストレインを用いた指標の中で,心室全体の収縮性を示す指標としてGLSが注目されている。GLSは,16分画で計測されたストレインを平均した値で,その中で長軸方向の収縮能を表す指標である。従来からGLSは,心機能の評価や予後予測に有効と言われているが,最近では冠動脈狭窄の存在診断に,安静時のGLSが役立つとも報告されている。GLSによる冠動脈狭窄の診断能を検討した10の論文をメタ解析した研究では,安静時にGLSが低下した場合に,有意な冠動脈狭窄を感度と特異度が70%台で予測可能と報告されている5)。ただし,平均GLSが冠動脈疾患ありで−16.5%,冠動脈疾患なしで−19.7%であり,その差が小さいことに留意すべきである。また,虚血性心筋症における検討では,GLSは特にischemic cardiomyopathyの予後予測に有用と報告されている6)。
Aplio i900では,“Auto EF”によってワンボタンでEFを自動計測できる機能が搭載されている。4 chamberと2 chamberでEFを計測するmethod of discs法を,ボタンを2回押すだけで計測できる優れた機能である。さらにAplio i900ではEFだけでなくGLSについても同時に算出可能で,従来煩わしさが先に立ってなかなか計測できなかったストレイン解析をサポートする機能となっている(図10)。
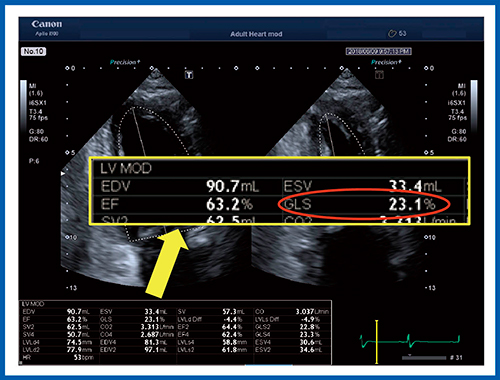
図10 GLSの自動算出
まとめ
Aplio i900では,ビームプロファイルの向上で繊細で良好なBモード画像の描出が可能になった。それをベースとして,虚血診断やPCIの適応決定に必要なCFRや負荷エコー,ストレイン解析が可能な機能を提供しており,日常臨床の中で遭遇する症例に役立つ可能性を感じている。
●参考文献
1)Hozumi, T., et al., Circulation, 97, 1557 〜1562, 1998.
2)Caiati, C., et al., J. Am. Coll. Cardiol., 34, 122〜130, 1999.
3)Daimon, M., et al., J. Am. Coll. Cardiol., 37, 1310〜1315, 2001.
4)Seo, Y., et al., JACC Cardiovasc. Imaging, 4, 358〜365, 2011.
5)Liou, K., et al., J. Am. Soc. Echocardiogr., 29, 724〜735, 2016.
6)Cho, G.Y., et al., J. Am. Coll. Cardiol., 54, 618〜624, 2009.

宮崎知奈美(Miyazaki Chinami)
1997年 大阪市立大学医学部卒業。同年,大阪市立大学医学部第一内科(現・循環器内科)に入局。多根総合病院を経て,2003年 Mayo Clinic Echocardiography Labに留学。2008年より東住吉森本病院循環器内科。
- 【関連コンテンツ】
