Deep Learning Reconstructionの新しい展開
大田 英揮(東北大学大学院医学系研究科 先進MRI共同研究講座)
MRI
2021-6-25

キヤノンメディカルシステムズの“Deep Learning Reconstruction(DLR)”である“Advanced intelligent Clear-IQ Engine(AiCE)”のMRIでの適用について,Ultra short TE(UTE)とdynamic撮像を中心に,当院での経験を紹介する。
DLRのMRIへの適用とアルゴリズムの特長
AiCEは,2018年に熊本大学,ボルドー大学との共同研究が始まり,2019年に製品化され臨床機へ搭載された。2019年の熊本大学とキヤノンメディカルシステムズの論文1)を嚆矢(こうし)として,以後,MRIへのDLRの適用は飛躍的に増加し急速な広がりを見せている。
AiCEでは,スキャン時間を延長せずにノイズを削減した画像を再構成によって取得できる。アルゴリズムの特長として,“Soft shrinkage activation functions”が挙げられる。機械学習などの人工知能(AI)技術ではブラックボックス化が問題になるが,Soft shrinkage activation functionsでは外部からパラメータを調整することで出力結果を変えることができる。これによって,さまざまなノイズ強度の画像に対して1つのネットワークで対応できるのが特長である。さらに最新のAiCEでは,g-factorによって空間的に変動するノイズを調整するパラメータが追加され,g-factor依存のノイズ低減が可能になった。
Ultra short TEへのDLRの適用
DLRの臨床応用について,最初にultra short TE(UTE)とTime-SLIP法を組み合わせた撮像法の検討を報告する2)。
腹部血管内治療後の血管評価のためのMRAでは,ステントなど金属デバイスのアーチファクトによって画質が低下し,血管内腔や近傍の評価が困難となる。
また,腹部血管の描出には,背景信号と血管内腔の良好なコントラストが重要である。キヤノンメディカルシステムズが開発した非造影Time-SLIP法では,選択的IRパルスで背景信号を抑制し,新たに流入する血液を“シャッタースピード”の速いTrueSSFP などで撮像することにより,腹部血管の描出が可能である。しかし,TrueSSFP Time-SLIP MRA(bSSFP Time-SLIP)では,位相分散効果による信号低下,磁化率アーチファクトの影響で,金属デバイス近傍の描出には限界がある。信号取得にUTEを用いることで,非常に短いTEによって磁化率効果,乱流の影響,ボクセル内の位相分散効果を最小限にでき,金属アーチファクトの低減が期待できる。
一方で,UTEではデータのサンプリング量が少なく,bSSFP Time-SLIPと同等の撮像時間ではtrajectoryが不足し,十分な画像が得られない。そこで,DLRを適用することで,信号対雑音比(SNR)の改善が可能かどうかを検証した。
denoising with DLR(dDLR)のアルゴリズムは,discrete cosine変換で高周波と低周波成分に分け,高周波部分にのみノイズ除去などの処理を行い画像を生成する。これによって,コントラストに大きな影響を与えずにSNRの改善が可能になる。
bSSFP Time-SLIPとほぼ同等の撮像時間のUTE Time-SLIPについて,dDLRの適用なしとありの画像,およびその差分画像を作成した。TrueSSFPではdDLRを適用しても差分画像にノイズはほとんど見られず,基本的な画質が良好だと考えられた。一方で,UTEではdDLRの適用で画質が向上し,差分画像でもノイズやストリークアーチファクトが激減していることがわかる(図1)。図2はボランティアで撮像した腹部画像だが,dDLRによる画像再構成で画質が大きく向上している。
bSSFP Time-SLIPとUTE Time-SLIPについて,10名のボランティアを対象に撮像した腹部画像を,dDLRの適用ありとなしで,SNR,コントラスト比,画質を比較した。SNRは,大動脈および腹部分枝では,UTE Time-SLIPではいずれの血管でも改善が見られた。一方で,bSSFP Time-SLIPでは有意差はなく,これは基本となるTrueSSFPの画質の良さと考えられた。コントラスト比については,血管内腔と筋肉で比較したところ,bSSFP Time-SLIPとUTE Time-SLIPのいずれもDLRの適用の有無にかかわらず,有意な変化はなかった。
腎動脈瘤に対するコイル塞栓後(図3)では,bSSFP Time-SLIP(b)では,治療後には腎動脈の背側枝の信号強度が低下して血流の確認が難しいが,UTE Time-SLIP(c)ではコイル近傍の信号低下がなく残存血流が明瞭に描出されており,このような血管内治療後の例ではUTE Time-SLIPの方が描出能が高いと思われる。
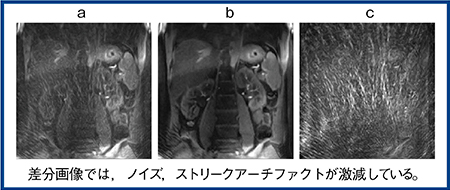
図1 UTE Time-SLIP with dDLR
a:dDLRなし b:dDLRあり c:差分画像
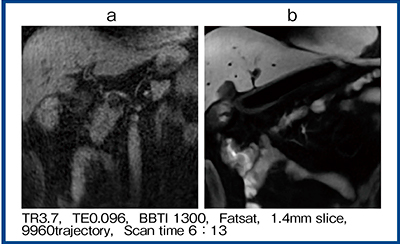
図2 ボランティアによるUTE Time-SLIP with dDLRの腹部画像
a:dDLRなし b:dDLRあり
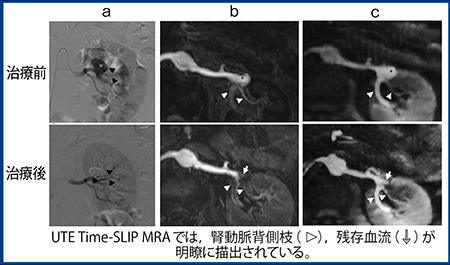
図3 臨床例:腎動脈瘤に対するコイル塞栓後
a:DSA b:bSSFP Time-SLIP c:UTE Time-SLIP
Dynamic DLR
次にdynamic撮像へのDLRの適用について述べる3)。
腹部のdynamic MRIは日常診療でさまざまな疾患で撮像されているが,息止め不良患者や小児などでは自由呼吸下での撮像が望ましい。自由呼吸下において,時間分解能とアンダーサンプリングによる画質低下のトレードオフを克服する方法として,convolutional neural network(CNN)に基づいた画像再構成について検証した。信号収集にはradial samplingの撮像法であるstack-of-starsを使用し,画像再構成としてtemporal-multi-resolution CNN(t-Multi CNN)4)を適用して画像の妥当性を検討した。対象は,当院でガドリニウム造影剤の使用が予定されていた肝疾患のない29例で,前向き研究として行われた。
t-Multi CNNでは,少ない枚数で時間分解能を向上させた“high-speed stack-of-stars acqusition”で得られた画像をトレーニングデータセットとしている。少ないスポーク数で再構成されるstack-of-stars画像では,ストリークアーチファクト低減のためview sharingを用いるが,時間分解能が低下し再構成画像がぼやけてしまう弊害がある。今回新たに提案したt-Multi CNNでは,時間分解能を向上させたデータセットを用いることで,時間分解能とview sharingによる空間解像度の向上を両立できる(図4)。図5は,t-Multi CNNを用いたdynamic撮像のMPR画像だが,撮像枚数50枚,スライス厚4mm程度,自由呼吸下で時間分解能の高い画像が得られている。
stack-of-starsで収集したデータをt-Multi CNNで再構成した画像と,4.5秒/1フレームの時間分解能でview sharingなし(No-VS),view sharingが5倍のlevel5を使った画像(VS5)を作成し,定量・定性評価を行った(図6)。
定量評価では,大動脈と肝実質にROIを設定したtime intensity curve(TIC)はNo-VSでカーブに上下動が見られた。大動脈のTICのtime to peak(TTP)とpeak enhancement(PE)ratioから求めた時間分解能の評価では,VS5でTTPが優位に延長した。これは時間分解能的な劣化を示していると考えられた。平衡相における肝実質のTICのstandard errorは,No-VSが有意に大きい結果であった。定性評価は,2名の放射線科医が画質評価および腹腔動脈分枝・門脈分枝描出の程度を5段階で評価した。血管描出の静的な評価では,VS5とt-Multi CNNが同等の評価となった。
t-Multi CNNの技術的側面として,compressed sensing(CS)を適用していないため計算負荷が少なく,今後,“real-time”reconstructionの可能性が期待できる。また,臨床応用では自由呼吸下の撮像に加え,灌流画像やDSAのような血流効果の評価が可能になることも期待される。
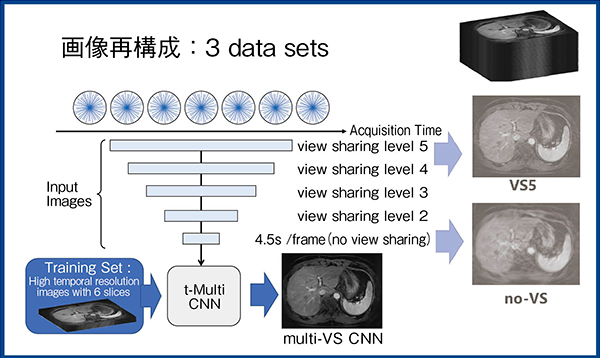
図4 t-Multi CNNによる画像再構成
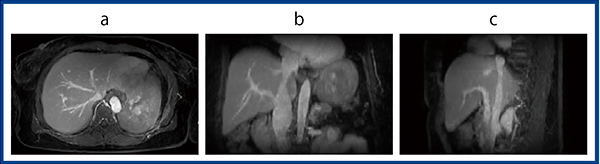
図5 t-Multi CNNによるdynamic MRI:3方向断面
a:axial b:coronal c:sagittal
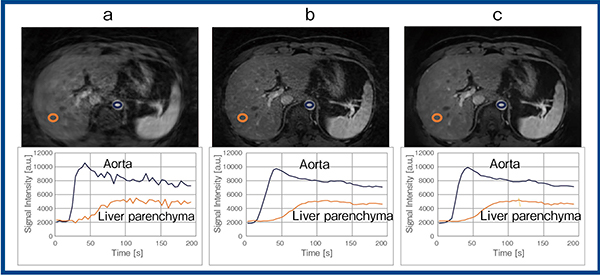
図6 t-Multi CNNの定量評価
a:No-VS(21spokes/frame) b:VS5(105 spokes/frame)
c:t-Multi CNN(21〜105 spokes/frame)
まとめ
DLRは,ノイズを低減しMRIの画質を飛躍的に向上させることが可能である。さらに,DLRを適用することで時間分解能と空間分解能のトレードオフという限界をなくし,新しいアプリケーションや撮像法の開発,患者負担の低減,さらには業務効率の改善なども期待できる可能性がある。今後,DLRを用いた画像再構成技術がMRIに標準的に搭載されることが望まれる。
* AiCEはノイズフィルタの設計段階でAIを用いた画像再構成です。
* 記事内容はご経験や知見による,ご本人のご意見や感想が含まれる場合があります。
●参考文献
1)Kidoh, M., et al., Magn. Reson. Med. Sci. ,19(3): 195-206, 2020.
2)Mori, R., et al., J. Magn. Reson. Imaging, 2020(Epub ahead of print).
3)Ota, H., et al., RSNA 2020.
4)Takeshima, H., et al., Proc. Intl. Soc. Mag. Reson. Med., 27 : #0467, 2019.
- 【関連コンテンツ】
