Aquilion ONEの中枢神経疾患への臨床応用:当院における経験
平井 俊範(熊本大学大学院生命科学研究部放射線診断学講座)
Session 3
2021-12-24

キヤノンメディカルシステムズの320列面検出器CT(Area Detector CT:ADCT)「Aquilion ONE」は,16cmの幅を一度に撮影できるため,心臓はもとより中枢神経領域においても非常に有用である。本講演では,当院での経験を踏まえ,Aquilion ONEの臨床応用として,(1) 脳動脈瘤の術前評価はCT Angiography(CTA)のみで十分か,(2) CT Perfusion(CTP)データからCTAが得られるか,(3) 脳腫瘍の術前評価においてMRIに付加する情報はあるか,(4) 脳深部刺激療法(DBS)術後評価に金属アーチファクト低減アルゴリズム“Single Energy Metal Artifact Reduction(SEMAR)”は有用か,という4つの臨床的疑問に関する研究1)〜4)を紹介する。
■脳動脈瘤の術前評価はCTAのみで十分か1)
CTAによる脳動脈瘤の術前評価について,術中所見をゴールドスタンダードとし,40症例の未破裂脳動脈瘤に対して前向きに検討した。
症例1は,40歳代,男性,右中大脳動脈(MCA)分岐部の動脈瘤である。CTAでは,術前精査において重要な瘤の形状,ネックの大きさ,親動脈(M1)との位置関係などが,術中写真とほぼ同様に描出されていた(図1)。
動脈瘤およびネックの形状について,CTAにおける読影者間一致率,およびCTA・術中所見の一致率を検討したところ,それぞれ88%,80%と非常に高かった。同様に,動脈瘤と親動脈との位置関係についても,読影者間およびCTA・術中所見の一致率は,それぞれ90%,88%と非常に高かった。また,脳外科医によるCTAでの術前評価の検討では,全例(40例)で外科的な合併症の発生はなく,38例(95%)についてはCTAにて有用な情報が十分に得られたとの評価であった。一方,2例(5%)においては,CTAでは動脈瘤から分岐する細い穿通枝が描出できておらず,追加の情報が必要であると評価された。
以上より,Aquilion ONEによるCTAでは,未破裂脳動脈瘤の術前評価にほぼ十分な情報を得られるが,動脈瘤から起始する細い穿通枝の描出が十分でないことがある点が限界点であると考えられた。
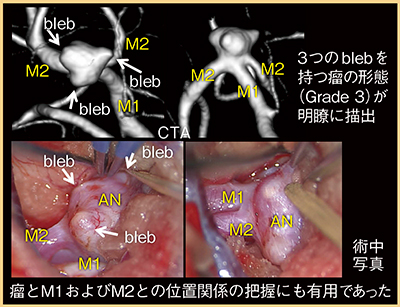
図1 症例1:CTAによる右MCA分岐部の動脈瘤の評価
(参考文献1)より引用転載)
■CTPデータからCTAが得られるか2)
通常,脳外科手術の術前・術後の評価においてはCTPとCTAの両方が撮影されるが,CTPのデータから十分なCTAを取得できれば,CTAの撮影を省くことができ,被ばく低減につながる可能性がある。そこで,当院にて脳動脈瘤のバイパス手術を行い,DSA(血管造影検査),CTP,CTAを撮影した7症例について前向きに検討した。
当院における頭部CTPの撮影プロトコールは,逐次近似応用再構成法“Adaptive Iterative Dose Reduction 3D(AIDR 3D)”を用いて1分間に20回の撮影を行い,単純CT,CTA,CT Venography(CTV),CTPを取得する。通常撮影は80kV,100mA,造影剤量50mLで行い,CTAは120kV,300mA,造影剤量50mLで撮影している。
症例2は,60歳代,女性,左内頸動脈瘤に対してSTA-MCAバイパス術を施行した症例である。図2は手術部位の反対側の画像であるが,Perfusion CTA(b)とConventional CTA(c)にてほぼ同等の情報が得られていた。
症例3は,60歳代,女性,左内頸動脈瘤術後の症例である。Conventional CTA(図3 c)では撮影タイミングが早く,末梢血管の描出が不良であるが,Perfusion CTA(図3 b)は複数の相から画像再構成を行うため,撮影タイミングに依存することなく末梢血管まで描出されている(図3←)。
Conventional CTA とPerfusion CTAの画質および血管描出能について,読影者による4段階評価の平均スコアを比較したところ,画質についてはPerfusion CTAの方が若干劣るものの,有意差は認めなかった。血管の描出能は,太い血管についてはいずれも非常に高スコアであった。末梢の血管については両者ともに描出能が低下するが,有意差は認めなかった。また,被ばくの平均は,Perfusion CTAが4.2mSv,Conventional CTAが3.1mSvであった。
以上より,Aquilion ONEのCTPのデータを用いてCTAの再構成は可能であり,撮影タイミングに依存せずに脈管情報を取得できる。Perfusion CTAは,細い末梢枝の描出に劣ることがあるが,Conventional CTAをおおよそ代替可能である。
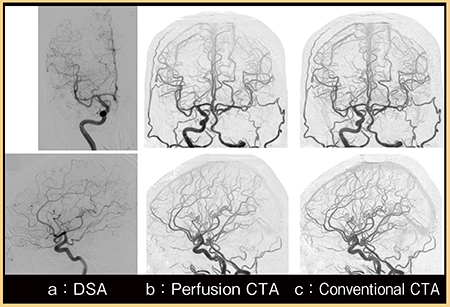
図2 症例2:Perfusion CTAとConventional CTAの画像比較
(参考文献2)より引用転載)
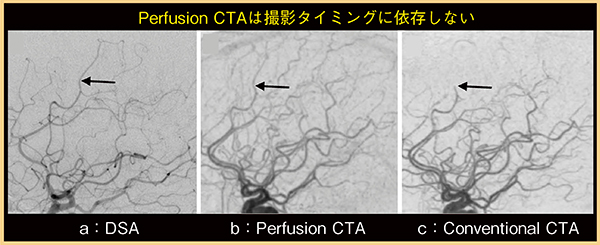
図3 症例3:Perfusion CTAとConventional CTAにおける末梢血管の描出能の比較
(参考文献2)より引用転載)
■脳腫瘍の術前評価においてMRIに付加する情報はあるか3)
Aquilion ONEのDynamic Volume Scanでは,CTA,CTV,CTPのデータが得られ,形態と機能を一度に評価可能である。脳腫瘍の術前評価は通常,MRIが第一選択となるが,特に脳実質内腫瘍に関してCTにて付加情報を得られるか検討を行った。
症例4は,60歳代,女性,膠芽腫である。MRAとCTAの比較では,末梢血管の描出はCTAの方が明瞭であった。また,MR Venography(MRV)・脳表画像のフュージョン画像(図4 a),およびCTV・CTA・脳表画像のフュージョン画像(図4 b)を比較すると,静脈走行の描出はCTの方が明瞭であり,脳外科医からは,腫瘍と血管との関係(図4 b↓)を明瞭に確認でき手術に非常に有用との評価であった。
流入動脈,静脈走行,腫瘍と周囲血管との位置関係の描出について,CTとMRIを比較したところ,ほぼすべての症例でCTはMRIと同等,もしくはCTの方が勝っていた。また,MR Perfusion(MRP)による脳血液量(CBV)の値は,CTPによるCBVよりも高い傾向であったが,MRPとCTPには高い相関が認められた。
脳外科医による術前評価において,MRIに対するCTの付加情報は16例中13例(81%)に見られ,そのうち5例については治療に非常に有益な情報が得られていた。5例の内訳は,富血管性腫瘍の切除に有用な血管情報取得が4例,脳実質内・実質外の鑑別に有用であったものが1例であった。
以上より,CTはMRIに対して血管系における付加情報を付与することができる。特に,富血管性腫瘍においては,動静脈と腫瘍との位置関係を把握でき,治療への有用性が高いと思われる。
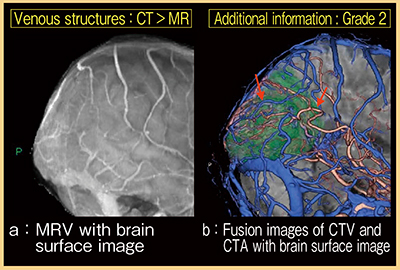
図4 症例4:MRV・脳表画像のフュージョン画像(a)およびCTV・CTA・脳表画像のフュージョン画像(b)の比較
(参考文献3)より引用転載)
■DBS術後評価にSEMARは有用か4)
SEMARは,Single Energyデータに対し,Forward projectionとBack projectionを複数回繰り返して金属アーチファクトを選択的に低減する手法である。
近年,パーキンソン病などの患者に多く行われているDBSでは,CT撮影を行うと強いアーチファクトが出現することが多い。そこで,DBS術後評価におけるSEMARの有用性を検討した。
症例5は,パーキンソン病の70歳代,女性に対し,両側視床下核にDBSを施行した症例である。SEMARの適用ありとなしの画像(図5)を比較すると,SEMAR適用ありではリード線近傍のアーチファクトが著明に低減している(b)。これにより,深部灰白質の陳旧性の血管障害と思われる低吸収域が明瞭となった(図5 b ↓)。SEMAR適用ありの方が頭頂側のアーチファクトがやや目立つが,これは脳表のリード線の影響であると考えられる。
定性評価を行ったところ,金属アーチファクトはSEMARを適用することで有意に減少し,脳の構造の描出能も有意に向上するという結果であった。
以上より,SEMARの適用によってDBS装置からの金属アーチファクトが低減され,脳実質の評価に有用である。
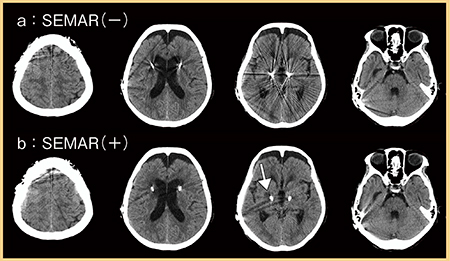
図5 症例5:SEMARの適用ありとなしの画像比較
(参考文献4)より引用転載)
■まとめ
Aquilion ONEの中枢神経疾患への臨床応用について,当院における経験を述べた。今後,Deep Learning Reconstructionである“Advanced intelligent Clear-IQ Engine(AiCE)”やDual Energy技術などを用いた臨床応用が期待される。
*AiCEは画像再構成処理の設計段階でAI技術を用いており,本システム自体に自己学習機能は有しておりません。
*記事内容はご経験や知見による,ご本人のご意見や感想が含まれる場合があります。
●参考文献
1)Hayashida, E., et al. , Jpn. J. Radiol., 31(9):600-607, 2013.
2)Kidoh, M., et al., Jpn. J. Radiol., 33(36): 353-359, 2015.
3)Hayashida, E., et al., Jpn. J. Radiol., 34(10): 691-699, 2016
4)Nagayama, Y., et al., Am. J. Neuroradiol., 41(2) : 231-237, 2020.
一般的名称:全身用X線CT診断装置
販売名:CTスキャナ Aquilion ONE TSX-305A
認証番号:227ADBZX00178000
一般的名称:全身用X線CT診断装置
販売名:CTスキャナ Aquilion ONE TSX-306A
認証番号:301ADBZX00028000
- 【関連コンテンツ】
