セミナーレポート(富士フイルムヘルスケア)
Ultrasonic Week 2019が,2019年5月24日(金)〜26日(日)の3日間,グランドプリンスホテル新高輪(東京都港区)にて開催された。26日に行われた株式会社日立製作所共催のランチョンセミナー11では,日本大学医学部附属板橋病院乳腺内分泌外科部長の櫻井健一氏を座長に,済生会松阪総合病院乳腺外科の柏倉由実氏と川崎医科大学総合医療センター外科部長 / 同大学総合外科学特任教授の中島一毅氏が,「乳腺超音波検査における今と今後」をテーマに講演した。
2019年9月号
Ultrasonic Week 2019 ランチョンセミナー11 乳腺超音波検査における今と今後
見直してみよう,超音波の基本〜物理苦手でもここまでは理解できた超音波の基礎〜
柏倉 由実(済生会松阪総合病院乳腺外科)
超音波検査を行っていると,通常よりも画像が見えづらいケースに遭遇することがある。本講演では,こうした日常臨床における問題の解決に役立つ超音波の基礎・基本について,物理特性なども踏まえて概説する。また,臨床で役立つ良好な画像をより簡便に得るために有用な,日立製の超音波診断装置「ARIETTA 850」のさまざまな技術を紹介する。
超音波の基礎・手技の基本
1.プローブ操作のポイント
物理的な側面から見ると,超音波は真っ直ぐに進み,その波が対象物に届いて反射波となり,プローブに戻って初めて信号となる。超音波が対象物に斜めに当たると反射波が屈折し,正しい信号が得られない。カラードプラやエラストグラフィなども同様で,プローブの当て方ひとつで診断結果が変わってしまうこともあることから,信頼性の高い画像を得るために,プローブを垂直に保った状態で当てるよう十分注意する必要がある。
正しいプローブの当て方として,力加減も重要である。プローブを強く押し当てすぎて一部が欠損しているような超音波画像では,乳腺境界線の断裂などが視認しづらくなる。超音波が対象物に届きさえすれば反射信号は得られるため,ハードゼリーなど信号を伝達できるものを介していれば,必ずしもプローブが皮膚と密着している必要はない。
2.超音波減衰とフォーカス
超音波は,生体の深部に進むほど減衰していく性質を持つ。そこで,超音波診断装置には,信号減衰を補正する機能としてSTC(sensitivity time control)またはTGC(time gain control)が搭載されている。また,減衰の程度は周波数にも依存する。プローブには低周波と高周波があるが,STCを変えずにフォーカスをそろえて画像を比較すると,深部では低周波プローブの方が良好な画像が得られる。
フォーカスの位置を変更することによっても,画像の印象は大きく変わる。超音波の波源のタイミングをずらすことで,診断装置はフォーカスの深度を変更しているが,超音波検査を行う際には,関心領域にきちんとフォーカスを合わせることは必須である。
最近の超音波診断装置はかなり改善されているものの,本来,超音波は浅部の病変にフォーカスを合わせづらい。そのような場合は,音響カプラーやハードゼリーを用いて物理的に距離を取ることで,浅部の病変でも明瞭に描出することが可能となる(図1)。
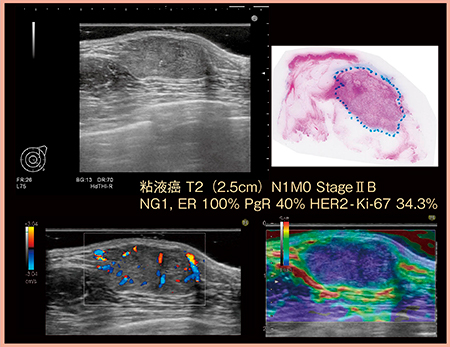
図1 浅部病変の良好な描出
3.設定の調整と追加情報の重要性
Bモードは,対象物の反射の強さを輝度(白さ)に変換して表示するが,超音波診断装置のモニタ上で表現できる色はわずか256階調であるため,反射の強さをどの段階の色に割り当てるかで画像の印象は変化する。コントラストの強さは,ダイナミックレンジ(DR)の幅を変化させることで調整可能であり,例えば,点状エコーはDRを狭くする(コントラストが強い)と視認しやすくなる。また,ゲインは反射信号の強さを調整可能で,ゲインを上げると弱い信号が増幅され,ゲインを下げると強い信号が増幅されるが,下げすぎると弱い信号が欠落する。このため,DRとゲインを適切に調整することが重要である。ほかにも,超音波診断装置にはさまざまなパラメータや補正フィルタが搭載されており,それらによって画像が見やすく調整されている。なお,症例ごとに設定を変えると評価が混乱するため,まずは標準の設定で評価した上で,状況に応じて調整していくことが重要である。
また,近年,Bモードの画質は飛躍的に向上しているが,それでも診断に迷う場合は,カラードプラによる血流の情報やエラストグラフィによる硬さの情報を見ることで,より正確な診断が可能となる。
臨床で役立つ先端技術
1.“eFocusing”と「4G CMUT」
従来の装置では,良好な画像を得るために,さまざまな工夫を要することがあったが(図2 a),日立製の超音波診断装置ARIETTA 850では,新しい送受信技術eFocusingと半導体技術を用いた超広帯域プローブ4G CMUTにより,工夫をしなくても容易に,きわめて良好な画像が得られるようになった(図2 b)。
従来の送受信方式では,送信ビームの中央部で数本のビームを受信し,順にスキャンして画像を描出していたが,eFocusingでは,送信ビームの中央部でより多くのビームを受信し,すべての深度で受信ビームの加算を行った上で画像化する。さらに,バックグラウンドの処理速度も高速化したことで,浅部から深部までフォーカスの合った画像がリアルタイムに表示可能となった。また,従来のプローブは,生体とのインピーダンスの差を音響整合層で小さくして音波を生体に浸透しやすくしていたが,4G CMUTでは音響整合層が不要となり,生体に対して理想的なパルスを送信することができる。
図3は,乳房下部に6cm大の腫瘤があり,周囲には浮腫性変化が認められるほか,アトピー性皮膚炎で表皮が荒れているなど,条件の厳しい症例であるが,eFocusingと4G CMUTを用いることで病変の内部まで描出が可能であった。
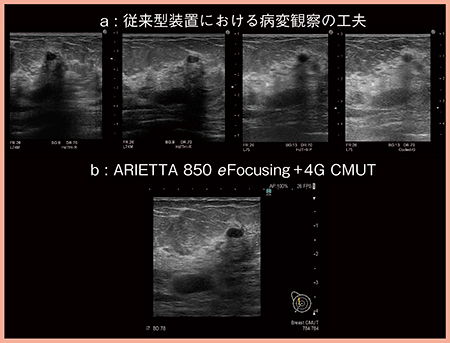
図2 eFocusingと4G CMUTでは良好な画像を容易に取得可能
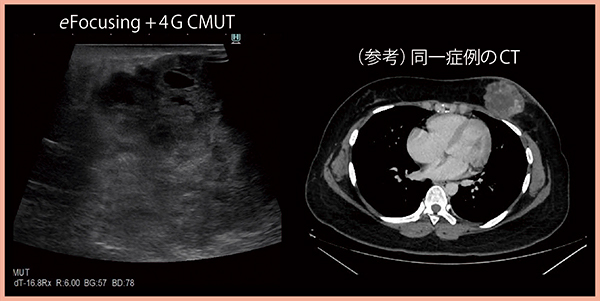
図3 eFocusingと4G CMUTによる病変の良好な描出(6cm大の乳房腫瘤)
2.Detective Flow Imaging(DFI)
DFIは,これまで描出困難であった低流速の血流を表示する技術で,従来はアーチファクトを除去することで消えてしまっていた微細な血流を残し,より高分解能かつ高感度に描出可能となった。
図4は,乳房内に膿瘍が見られた症例の反応性リンパ節で,カラードプラでもリンパ門側からの血流が描出されているが(a),DFIでは樹枝状の微細な血流が明瞭である(b)。
図5は乳がん症例で,カラードプラ(b)にて貫入する血流が認められるが,DFI(c)ではより詳細に血流を評価できる。
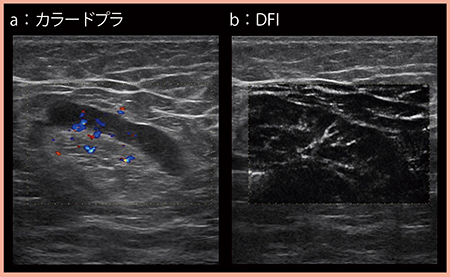
図4 DFIによる微細血流の描出(反応性リンパ節)
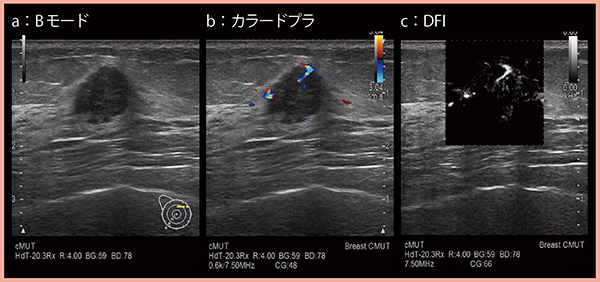
図5 DFIによる微細血流の描出(乳がん)
まとめ
超音波検査を行うに当たっては,超音波の基本を押さえて設定を調節することで,得られる情報を増やすことが可能である。また,技術の進歩によって画像がより見やすくなる反面,従来は見えていなかったものが見えるようになり,戸惑うこともあるかと思われる。しかし,超音波の特性や診断装置の性質への理解を深めて生かすことができれば,より良い検査が行えるようになると考える。

柏倉 由実(Kashikura Yumi)
2005年 三重大学医学部卒業。済生会松坂総合病院にて初期・後期臨床研修。2008年 三重大学医学部附属病院乳腺外科。2015年 筑波メディカルセンター病院乳腺科。2017年〜済生会松坂総合病院乳腺外科。
- 【関連コンテンツ】
