ACCURAY RT UPDATE
2023年2月号
がん放射線治療の今を知る!~最前線の現場から No.4
「Radixact Synchrony」を用いた体幹部定位放射線治療の実際
原田 英幸(静岡県立静岡がんセンター放射線・陽子線治療センター放射線治療科部長)
新規放射線治療装置「Radixact」の導入
当院において,リニアック1台を更新するに当たり,強度変調放射線治療(IMRT)専用機であり,かつ動体追尾機能(Synchrony)が新たにオプション搭載されたTomoTherapy最新プラットフォーム「Radixact」(アキュレイ社製)を導入することになった。本システムは,フィデューシャルマーカーを用いる方法だけでなく,マーカーレスでの肺腫瘍の動体追尾照射が可能である。2020年に導入後,同年11月より臨床使用を開始し,頭頸部がんを中心としたIMRTとともに,体幹部定位放射線治療(SBRT)でも臨床使用を開始している。本稿では,SBRTにおける動体追尾照射に焦点を当て,その初期経験を報告したい。
Radixact Synchronyによる動体追尾照射
動体追尾照射を行うためには,体表面と体内部の動きの2つの動体情報を取得する必要がある。体表面の動きの情報は,天井に設置されたSynchronyカメラを用いて,患者の体表面に装着したLEDマーカーの動きを検出することで呼吸位相の情報として取得する(図1)。一方,体内部の動きの情報は,治療ビームガントリから90°の位置に新たに搭載されたkV管球を用いて,X線画像(kV X線画像)を取得する。肺腫瘍自体あるいはフィデューシャルマーカーを継続的に撮影することで,体内部の動きを経時的に検出し,位置情報として取得する。
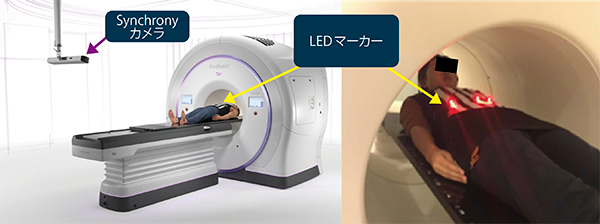
図1 Synchronyカメラによる呼吸性移動の評価(画像提供:アキュレイ株式会社)
動体追尾照射の仕組み
動体追尾照射に当たっては,ガントリ内で複数方向から連続的にkV X線画像を取得する。同時に,体表面の動きにより呼吸位相をモニターし,呼吸位相と腫瘍位置に関する相関モデルを作成する。実際の治療では,それぞれの呼吸位相で想定される腫瘍位置に照射されるとともに,照射中もkV X線画像取得により実際の腫瘍位置をモニターする。想定される腫瘍位置と実際に観察された腫瘍位置のズレが一定時間継続した場合,照射は中断され,再度相関モデルを作成した上で,照射を再開する(図2)。
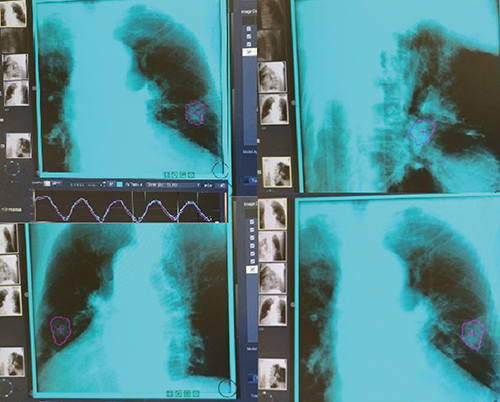
図2 照射中のkV X線画像
呼吸位相の情報と併せて,複数の方向から断続的にkV X線画像を取得し,腫瘍位置を自動認識する。
追尾精度の確認
1.広義のセットアップマージン
Radixact Synchronyでは,ターゲット自体を追尾するため,inter/intraセットアップエラーは原理的には補正される。ただし,腫瘍とフィデューシャルマーカーの動きが異なる場合は,その乖離について考慮する必要がある。一方,装置の幾何学的エラーは日々の品質管理の結果から,1mm以下と見積もった。
2.Radixact Synchronyに関するマージン
ターゲットの認識・追尾の不確かさは1.5mm程度と報告されている1),2)。当院でのコミッショニングでも,動体追尾照射の線量プロファイルに2mm以内のズレが観測された。また,三次元的な呼吸モデルの不確かさ,モデルと腫瘍位置の差をそれぞれ最大3mmまで許容する設定とした。さらに,頭尾方向はjawコリメータによる連続的な追尾であるのに対し,左右・腹背方向はバイナリー・マルチリーフコリメータによる段階的な追尾となる。これらすべての因子を鑑み,確実な計画標的体積(planning target volume:PTV)マージンを設定することとし,原則5mmの設定で臨床を開始した。
肺腫瘍に対するマーカーレス動体追尾照射の初期経験
肺腫瘍に対する動体追尾によるSBRTの初期経験を報告したい。従来当院では,自由呼吸下の内的標的体積(internal target volume:ITV)法によるPTV設定,あるいは体表面の赤外線マーカーの動きに連動した呼吸同期照射を実施していた。Radixact Synchronyによる動体追尾照射も,基本的な患者フローは従来と同様で,CTシミュレーションを実施して治療計画を作成後,患者に来院してもらい照射を開始するという流れになる。そこに新たに追加されたのが,「Synchronyシミュレーション」である。これは,いわゆる「治療リハーサル」に当たるプロセスであり,動体追尾が実際に可能かどうかの事前確認となる(図3)。治療ビームこそ出ないが,腫瘍認識および相関モデル作成の一連のプロセスを,患者に寝台上で治療体位をとってもらい,実際に撮影を行って確認する。特に,肺腫瘍ではマーカーレスでの追尾を行うに当たり,腫瘍が認識できるか,また,認識した腫瘍の動きに追尾した照射が可能かを事前に確認する。実際に,一部で腫瘍認識が不可,あるいは呼吸が安定しないなどの理由で追尾が不可であり,動体追尾以外の方法による定位照射に切り替えた症例があった(図4)。
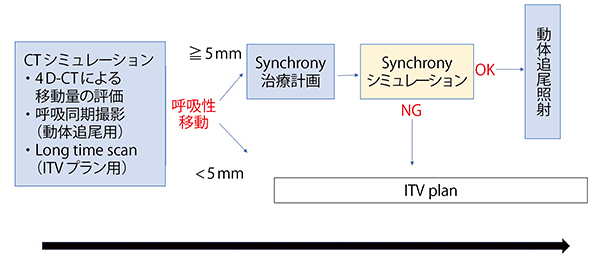
図3 当院のSynchrony治療の診療フロー
CTシミュレーションの結果,呼吸性移動が5mm以上の場合は動体追尾照射を検討する。Synchronyシミュレーションを行い,事前に動体追尾照射適応の可否を判断する。
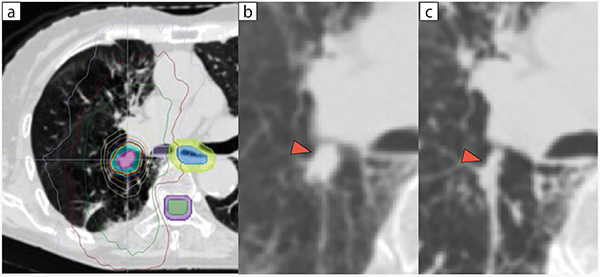
図4 動体追尾照射困難例
a:線量分布図,b:治療前のCT(▶腫瘍),c:照射期間中のCT(▶腫瘍)
腫瘍縮小(c▶)により,動体追尾照射の継続が困難であった。
腹部腫瘍に対する動体追尾照射の初期経験
当院では,Radixact Synchrony導入を契機に,腹部腫瘍に対する定位照射を開始した。原発性肝がん,腎がん,前立腺がんだけでなく,オリゴ転移に対する定位放射線治療が保険収載されたことにより,各腹部臓器への定位照射のニーズが高まっている。腹部腫瘍では,腫瘍そのものをkV X線画像で認識できないため,フィデューシャルマーカーが必須である(図5)。特に上腹部病変の場合では,腫瘍は呼吸性に移動することから,動体追尾照射を行うことでPTVとリスク臓器の重複体積を減少することができる。
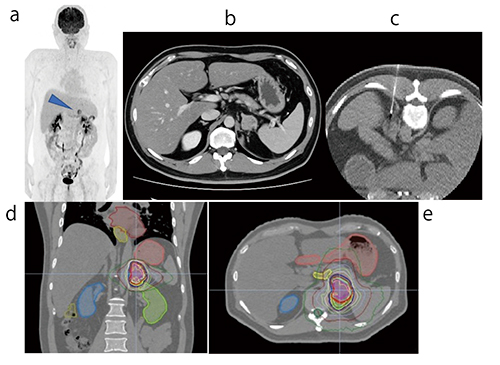
図5 副腎腫瘍に対する動体追尾照射例
FDG-PET画像では副腎のみのオリゴ転移であった (a▶,b)。フィデューシャルマーカー挿入後に,動体追尾での定位照射を実施した(d,e)。なお,副腎腫瘍でのフィデューシャルマーカーは適応外使用となる(c)。
臨床使用経験のまとめと今後の課題
動体追尾照射はSBRTにおいて,腫瘍およびリスク臓器線量の観点から,原理的には最も優れた治療法である。当院での動体追尾照射の実施症例では,位置誤差などすべての要素を包含したPTVマージンを5mmと設定し,一連の治療が可能であった。特に,呼吸性移動が大きい腫瘍に対しては,魅力的な治療法であるのは言うまでもない。一方,一部ではあるが追尾が困難な場合があり,事前のSynchronyシミュレーションを行うことの必要性を再確認した。また,PTVマージンを5mm以下にできるかどうかは検討課題であるが,安静呼吸下での呼吸性移動が5mm以下の腫瘍では,動体追尾照射のメリットは少なく,ITV法を用いることが良い場合もある。そのため,動体追尾照射を適応する患者とそうでない患者を,CTシミュレーション施行後早期に判断することが求められる。
●参考文献
1)Ferris, W. S., et al. : Evaluation of radixact motion synchrony for 3D respiratory motion : Modeling accuracy and dosimetric fidelity. J. Appl. Clin. Med. Phys., 21(9): 96-106, 2020.
2)Chen, G.P., et al. : Comprehensive performance tests of the first clinical real‐time motion tracking and compensation system using MLC and jaws. Med. Phys., 47(7): 2814-2825, 2020.
