VARIAN RT REPORT
2022年3月号
人にやさしいがん医療を 放射線治療を中心に No.8
これまでのRapidPlan研究とビッグモデル作成の取り組みについて
門前 一(近畿大学医学部放射線医学教室放射線腫瘍学部門)
はじめに
多岐にわたる分野で利用されている人工知能(AI)は,放射線治療分野においても目を見張る進歩がある。AIを用いた知識ベース放射線治療計画(knowledge-based planning:KBP)は,すでに商業用の放射線治療計画装置「Eclipse」(バリアン社製)に実装されており,それが“RapidPlan(RP)”である。治療計画作成時の最適化を簡略化して治療計画時間を短縮するとともに,今までの治療計画と同等以上の線量分布の作成を多くの治療部位で可能としている1)〜7)。本稿では,RPの概要と種々の研究成果,ビッグモデル作成までの経緯について解説する。
RapidPlanについて
RPの概要を図1に示す。まず,強度変調放射線治療(IMRT)や強度変調回転放射線治療(VMAT)の治療計画をデータベースに登録する。そして,症例の解剖学的な情報と治療計画の照射野ジオメトリから簡易的に線量分布を計算し,また同様に,予測される線量体積ヒストグラム(DVH)であるGEDVHを取得する。GEDVHと実際の線量分布のDVHの特徴を主成分分析を用いて抽出し,登録した治療計画に対して,横軸をGEDVHの成分,縦軸をDVHの成分としてプロットした散布図から回帰直線を導き,RPモデルを作成する。
新規の症例に対して,治療計画用CTを基に解剖学的な位置情報と照射野ジオメトリからGEDVHを取得し,回帰直線から各リスク臓器(OAR)の達成可能なDVH(estimated DVH)を予測する。この予測された帯状のestimated DVHの下端に沿って,自動的に最適化条件であるline objectiveと優先度が設定され,最適化計算が行われる(図2)。
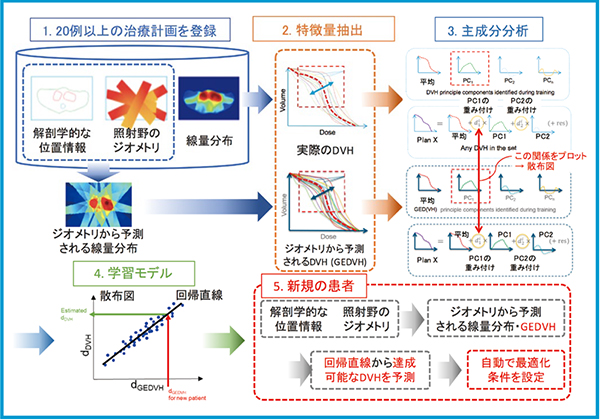
図1 RapidPlanの仕組みの概要
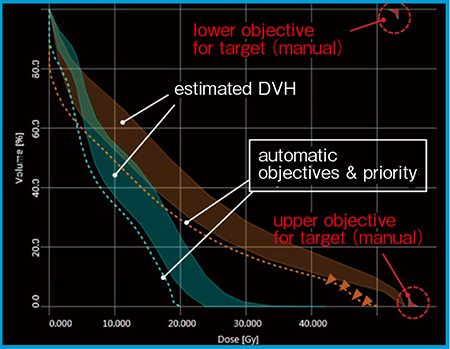
図2 RapidPlanによる達成可能なDVHと最適化条件の例
RapidPlanの学習モデルから達成可能なDVH(estimated DVH)を予測し,帯状に表示された下端のDVHに沿うようにline objectivesと優先度が自動的に設定される。ターゲットに関しては,手動でupperとlower objectivesを設定する必要がある。
RapidPlan研究の経緯
IMRTやVMATの治療計画では,ターゲットや各OARに対して,目標となる線量指標や制約の優先度をコンピュータに入力し,最適化計算を行う。しかし,この過程は計画者の経験やスキルに依存するため,治療計画の質が計画者間や施設間で異なることや,試行錯誤を繰り返すために時間を要するという問題がある8)。これらの問題に対して,RPは治療計画時間の短縮や,計画者間や施設間における治療計画の標準化が期待できると考えられている。
われわれは,前立腺がん症例を対象に,過去に施行したIMRTとVMATの治療計画50例を登録して,RPモデルの作成を行った。所要時間はわずか30分であった。そのRPモデルを使用して,一度のみの最適化計算で過去に施行した治療計画と同等以上の線量分布が得られたこと3),さらには,その線量分布と過去の治療計画の線量分布の違いを指摘できるスタッフが皆無であったことを記憶している。
次のステップとして,RPモデルを他施設に提供することで,施設間の治療計画の質のバラツキも低減でき,標準化の一助となりうると期待を込めて研究を進めた。しかし,RPモデルが作成する治療計画は,RPモデルを作成した施設の処方の方法や線量,OARの線量制約といったプランポリシーを如実に反映するため,他施設でのRPモデルの使用では,1回の最適化計算でその施設のクライテリアを満たすことができない症例が少なくなかった。最適化の過程においても,もう一手間が必要となり,他施設に提供した際は納得できる結果を得られず,治療計画の質の均てん化や標準化におけるRPの使用には壁を感じた9)。
ビッグモデル作成への取り組み
Schubertらは,ある1つの施設の治療計画43例をデータベースに登録して作成したRPモデルを7施設に共有したところ,すべての施設において臨床使用可能であったと報告している10)。これらの7施設はプランポリシーをそろえており,contouringがRPモデルに登録した症例と大きく異なる場合には,手動による調整が必要と考察している。このことから,この手法でのRPモデルの作成では,計画者や施設の主観性が残っていることがわかる。また,Panettieriらは,8施設から収集した前立腺がんに対する治療計画110例をRPモデルに登録したところ,多施設多種のデータを登録したRPモデルは,参加施設では共有使用可能であるが,参加施設外への共有には不向きであったとも述べている11)。これも先述同様に,グループ内で決められた線量制約を満たしていることが条件となっており,このことが参加施設外への共有が不向きな要因となった可能性がある。
このような背景から,線量制約などの条件を設けず,プランポリシーの異なる多施設多種の治療計画を登録したRPモデルの有用性の検討が必要と認識し,ビッグデータに着目した。放射線治療計画においても,登録する治療計画のバリエーションや数を増やしビッグデータを活用したRPのビッグモデルを作成することのメリット・デメリットを施設間で共有可能か,また,治療計画の質の均てん化や標準化につながるかなどの視点から進めた。ビッグモデルでは,施設固有のRPモデルより,多様な解剖学的特徴や照射野ジオメトリ等々を学習できる。そのため,ビッグモデルによるestimated DVHから設定されるline objectiveは,OARの線量を効率的に低減できると考えられる。
共同で研究を行っている5施設9)から,前立腺がんに対するIMRTとVMATの治療計画,合計561例をデータベースに登録し,ビッグモデルを作成した。図3に,モデルの散布図と回帰直線の例を示す(図3 aが単施設のモデル,図3 bがビッグモデル)。各施設から,それぞれ150,153,49,60,149例をすべて匿名化してから出力し,登録作業を行ったが,一昼夜を要した。登録したすべての治療計画は,おのおのの施設において臨床使用されたものであり,各施設のプランポリシーを反映している。現在,同一症例に対して,ビッグモデルと,各施設が独自に作成したRPモデルが作成する線量分布・DVHを比較検討中であるが,ビッグモデルは,単施設のRPモデルと同等以上の線量分布・DVHを作成できている。ただし,ビッグモデルにも課題は残されている。例えば,図1に示した散布図において,プロット数(治療計画の登録数)が多くなりすぎて外れ値が増加してしまうことである。外れ値が多くなると回帰直線に影響を及ぼし,RPモデルの予測精度が下がり,納得できる線量分布が得られないとの報告がある12)。このような場合には,図3 cのように,登録データから外れ値を除外(clean-up)する工夫が必要である。
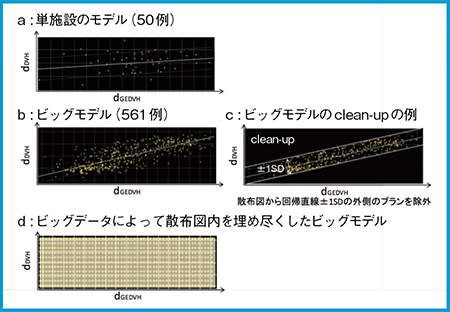
図3 RapidPlanモデルの散布図と回帰直線の例
aは単施設のモデル,bはビッグモデル,cはビッグモデルからclean-upを行った例,dは散布図を埋め尽くすようなビッグモデルの例。
おわりに
これまでのRPの研究経緯,およびビッグモデル作成の取り組みについて解説した。将来的には,世界中の治療計画(照射野ジオメトリ,線量分布)のデータを登録してビッグモデルを作成・共有することで,治療計画の質の担保に加え,標準化につながることが期待できる。また,図3 dに示すような散布モデルの作成や活用ができれば,最適化作業が無用の長物となる可能性があり,オンライン適応放射線治療がより現実的になるのかもしれない。
●参考文献
1)Tol, J.P., et al., Int. J. Radiat. Oncol. Biol. phys., 91(3) : 612-620, 2015.
2)Fogliata, A., et al., Radiat. Oncol., 10 : 220, 2015.
3)Kubo, K., Monzen, H., et al., Phys. Med., 44 : 199-204, 2017.
4)Ueda, Y., et al., Acta. Oncol., 59(3) : 274-283, 2020.
5)Uehara, T., Monzen, H., et al., J. Radiat. Res., 61(3) : 499-505, 2020.
6)Inoue, E., Monzen, H., et al., In Vivo. 34(3) : 1095-1101, 2020.
7)Wada, Y., Monzen, H., et al., J. Med. Phys., 46(1) : 7-15, 2021.
8)Nelms, B.E., et al., Pract. Radiat. Oncol., 2 : 296-305, 2012.
9)Ueda, Y., et al., Radiat. Oncol., 13 : 46, 2018.
10)Schubert, C., et al., PLos One, 12 : e0178034, 2017.
11)Panettieri, V., et al., Phys. Imaging Radiat. Oncol., 11 : 34-40, 2019.
12)Delaney, A.R., et al., Int. J. Radiat. Oncol. Biol. Phys., 94 : 469-477, 2016.
