VARIAN RT REPORT
2022年7月号
人にやさしいがん医療を 放射線治療を中心に No.10
頭頸部および婦人科領域におけるVelocityの臨床利用
佐々木幹治(徳島大学大学院医歯薬学研究部放射線治療学分野)
はじめに
画像誘導放射線治療装置を搭載した直線加速器の普及に伴い,画像データをさまざまな局面で利用する機会が増加した。また,近年では,放射線治療における画像データを効率的に利用するため,非剛体レジストレーション(deformable image registration:DIR)機能を有する放射線治療計画支援装置の利用が急速に広まった。これらの状況を鑑み,国内においては,「放射線治療における非剛体画像レジストレーション利用のためのガイドライン2018年版」が公開された1)。その後,2020年12月には,臨床現場で使用する場合の技術的・臨床的問題の注意点や疑問点の解決の一助として,『詳説 非剛体レジストレーション─放射線治療領域─』が発刊された2)。ただし,国内における放射線治療計画支援装置の使用状況を調査した報告3)では,装置は保有しているが臨床利用していない施設が19%,装置を保有していない施設が32%であった。したがって,国内の現状では,DIR技術は十分に普及した治療技術でないことが推察される。
本稿では,徳島大学病院における放射線治療計画支援装置「Velocity」(バリアン社製)の活用の一例として,頭頸部および婦人科領域に対するDIRの臨床利用について解説する。
頭頸部領域に対するDIRの臨床利用
徳島大学病院では,頭頸部領域の初回の治療計画時に予防的リンパ節領域およびリスク臓器(OAR)の自動輪郭抽出や,再治療計画時に初回治療計画時に使用した臨床的標的体積(CTV)およびOARの輪郭をプロパゲーションするDIR技術を最も頻繁に利用している。頭頸部領域に対する自動輪郭抽出機能を使用した先行研究では,手動による輪郭描出と比べて30〜50%の時間短縮につながったことが報告されている4),5)。また,自動輪郭抽出機能を使用することによって,作業者間の輪郭描出のバラツキの低減に有用であることも報告されている6)。自動輪郭抽出の手法には,セグメンテーションとプロパゲーションがある。Velocityの自動輪郭抽出には,セグメンテーション機能が搭載されており,異なる患者データ(CT画像および輪郭データ)に基づき,自動で輪郭を抽出する方法が採用されている。また,Velocityではアトラスベースのセグメンテーションの中でも,登録された複数のCT画像と輪郭データのセットから1種類のCT画像と輪郭データのセットが選択されるシングルアトラス法が採用されている。図1に,シングルアトラス法の概念図を示す。
続いて,再治療計画時において利用される輪郭のプロパゲーションについて解説する。再治療計画で時間を要する工程の一つとして,標的およびOARの輪郭の描出があり,DIRを用いた輪郭のプロパゲーションを行うことで,作業者間による輪郭描出のバラツキを低減することが可能となる。具体的には,同一患者の初回のCT画像と再治療計画CT画像を用いてDIRを実施することで,初回の輪郭データを再治療計画CT画像上に変形させて抽出する作業である。ただし,自動輪郭抽出も同様であるが,DIR実施後に作業者が再度の輪郭確認および修正を行うことが必須である。
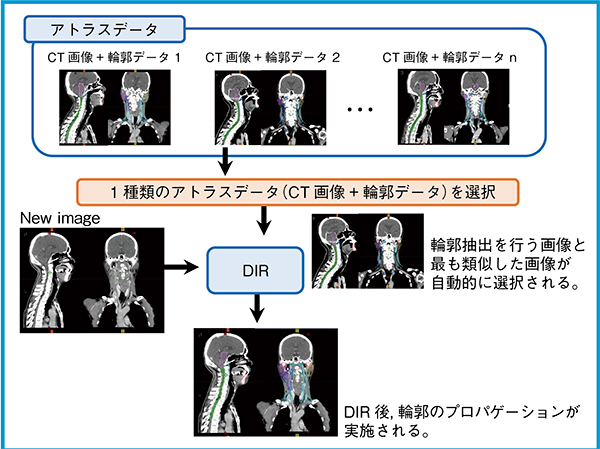
図1 シングルアトラス法の概念図
婦人科領域に対するDIRの臨床利用
画像誘導密封小線源治療(IGBT)における標的およびOARの輪郭描出を実施する上では,優れた軟部組織描出能を有するMRIの有用性を示す報告がある7)。また,欧州放射線腫瘍学会の婦人科腫瘍グループ(GEC-ESTRO working group)の提言によれば,IGBTを成功に導くためには,MR画像が果たす役割は非常に重要であることが示されている8)。さらに,MR画像を利用することで,輪郭入力の作業者間の違い(バラツキ)についても低減することが可能であると報告されている9)。ただし,国内の現状では,毎回のIGBTでMR撮像を行っている施設はきわめて少ない10)。徳島大学病院においても,MRI装置の臨床使用のオーダ枠の制限上,IGBTごとのMR撮像は行っていない。この課題を解決するため,事前に撮像したMR画像を用いて描出した肉眼的腫瘍体積(GTV)と高リスクCTV(HR-CTV)をIGBT用の治療計画用CT画像へプロパゲーションすることで,GTVとHR-CTVの輪郭を取得している。2回目以降のIGBTでは,初回IGBTの治療計画用CT画像に描出した輪郭をプロパゲーションすることで,効率的な輪郭描出に努めている。
外照射と密封小線源治療の線量評価では,これまで単純な線量加算(dose addition法)が利用されてきた。ただし,これらの条件が成立するためには,治療セッション間で内部臓器の位置および形状が一定であることや,治療セッション間でOARのホットスポットが一定であることなどが挙げられる。また,近年では,外照射と密封小線源治療の線量評価を行う上で,さまざまな取り組みが行われている。その一つとして,DIR技術を応用し,1種類のCTもしくはMR画像上で,複数の治療計画の線量合算を評価する手法(dose accumulation法)が用いられるようになってきた(図2)。Velocityに搭載されているDIRアルゴリズムは,強度ベースDIRとstructure guided DIRの2種類がある。structure guided DIRでは強度ベースDIRと比較し, DIR精度を向上させる報告が多数ある。ただし,DIR技術においては,腫瘍の縮小,膀胱の蓄尿量や直腸の状態(ガスや便の充填度合い),アプリケータの挿入の有無によって生じる複雑かつ大きな臓器変形によって,線量合算への利用が困難な場合があると考えられている11)。したがって,現状のDIR技術では,外照射と密封小線源治療の線量合算を扱うdose accumulation法は,まだ十分にロバストな手法ではないことが報告されている11)。今後,DIR技術は,臨床成績とこれらの関係性が明確になることで,急速に普及しうる技術であると考えている。
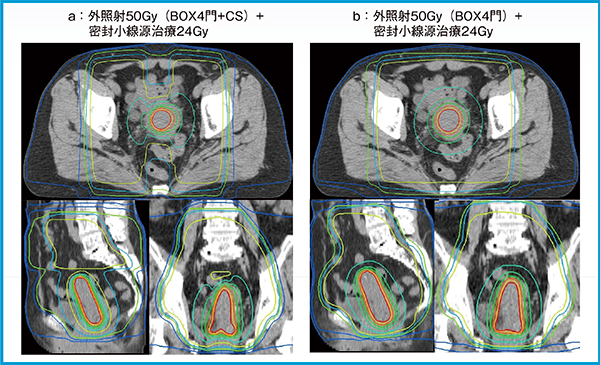
図2 Velocityを用いた外照射と密封小線源治療の線量合算の例
aは外照射〔BOX4門照射で30Gy照射後にセンターシールド(CS)による前後対向2門20Gy〕と密封小線源治療(HR-CTVに対してD90%で24Gy),bは外照射(BOX4門照射で50Gy)と密封小線源治療(HR-CTVに対してD90%で24Gy)の線量合算の例
おわりに
本稿では,徳島大学病院におけるVelocityの臨床利用として,頭頸部および婦人科領域における自動輪郭抽出,輪郭のプロパゲーション,外照射と密封小線源治療の線量合算における注意点や課題について解説を行った。将来的にはDIR技術は,人工知能(AI)技術の発展に伴い,その役割が代替される可能性もあるが,多くの先行研究に基づくエビデンスが存在する。ぜひ,Velocityを利活用いただき,明日からの臨床現場で効率的な放射線治療に役立てていただければ幸いである。
●参考文献
1)放射線治療における非剛体画像レジストレーション利用のためのガイドライン2018年版.
https://www.jastro.or.jp/medicalpersonnel/guideline/dir_v3.pdf
2)詳説 非剛体レジストレーション─放射線治療領域─. 角谷倫之 監修, 木藤哲史, 他編, 中外医学社, 東京, 2020.
3)Kadoya, N., et al. : Factual survey of the clinical use of deformable image registration software for radiotherapy in Japan. J. Radiat. Res., 60(4) : 546-553, 2019.
4)Ramadaan, I.S., et al. : Validation of Varian's SmartAdapt® deformable image registration algorithm for clinical application. Radiat. Oncol., 10 : 73, 2015.
5)Walker, G.V., et al. : Prospective randomized double-blind study of atlas-based organ-at-risk autosegmentation-assisted radiation planning in head and neck cancer. Radiother. Oncol., 112(3) : 321-325, 2014.
6)Chao, K.S., et al. : Reduce in variation and improve efficiency of target volume delineation by a computer-assisted system using a deformable image registration approach. Int. J. Radiat. Oncol. Biol. Phys., 68(5) : 1512-1521, 2007.
7)Viswanathan, A.N., et al. : Computed tomography versus magnetic resonance imaging-based contouring in cervical cancer brachytherapy : Results of a prospective trial and preliminary guidelines for standardized contours. Int. J. Radiat. Oncol. Biol. Phys., 68(2) : 491-498, 2007.
8)Dimopoulos, J.C., et al. : Recommendations from Gynaecological (GYN) GEC-ESTRO Working Group (IV) : Basic principles and parameters for MR imaging within the frame of image based adaptive cervix cancer brachytherapy. Radiother. Oncol., 103(1) : 113-122, 2012.
9)Dubois, D.F., et al. : Intraobserver and interobserver variability of MR imaging- and CT-derived prostate volumes after transperineal interstitial permanent prostate brachytherapy. Radiology, 207(3) : 785-789, 1998.
10)Ohno, T., et al. : A questionnaire-based survey on 3D image-guided brachytherapy for cervical cancer in Japan : Advances and obstacles. J. Radiat. Res., 56(6) : 897-903, 2015.
11)Swamidas, J., et al. : Image registration, contour propagation and dose accumulation of external beam and brachytherapy in gynecological radiotherapy. Radiother. Oncol.,143 : 1-11, 2020.
