VARIAN RT REPORT
2019年11月号
がん医療における放射線治療最前線 No.6
“RapidPlan”の臨床活用 〜経験を活かし共有する〜
大橋俊夫*1/深田恭平*2/池島健吾*1(*1 慶應義塾大学医学部放射線治療科 *2 慶應義塾大学医学部腫瘍センター)
放射線治療計画の現状と課題
強度変調放射線治療(IMRT)は,照射に用いるビームのフルエンスを最適化することにより,任意の複雑な形状の線量を投与することを可能とする。IMRTの治療計画では,さまざまな線量制約を用いて線量分布の最適化を行うが,どのような制約を使えばベストな分布が得られるかについては計画立案者により到着点が異なる。
治療計画の複雑化により,例えば,一人の患者に対して複数の計画立案者がいれば立案者の数だけ輪郭描画,治療計画が存在することになる。これらのバラツキを抑えるために近年着目されているのが,knowledge-based(知識ベース)による計画立案ツールである。バリアンメディカルシステムズが提供している放射線治療計画システム「Eclipse」では,過去の治療計画を参照して計画立案するツールとして“RapidPlan”が実装されている。
RapidPlanの概要
RapidPlanはIMRT/強度変調回転放射線治療(VMAT)の治療計画に特化しており,各患者にとって最適な治療計画を立案するために,過去の治療計画をベースに患者ごとに最適化条件を定義する機能を有している。あらかじめ設定した部位ごとの計画モデルを利用することで,過去の臨床治療を応用し,効率および品質を大幅に向上させることが可能である。
RapidPlanは,モデルの設定とdose volume histogram(DVH)の予測の2つのコンポーネントから構成されている。モデルは,過去に治療を行った計画をパラメータ化したものを基としている。構造セットと線量マトリックス,そして,DVH,ターゲットとリスク臓器の相関位置関係などを解析し,モデルに学習させる。最低30症例が必要であるが,モデルに組み込む治療計画が多いほど精度が増すとされている。登録したモデルを新規患者の治療計画で使用することにより,DVHの予測(図1)を行い,過去の治療計画に則った最適化条件の設定を実現する。
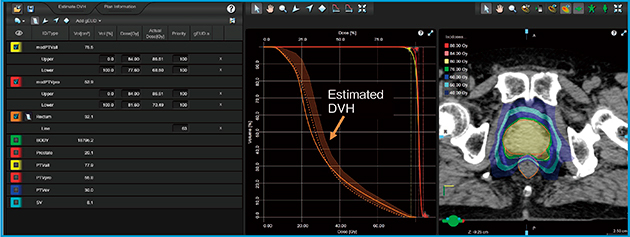
図1 RapidPlanを用いて計算した予測DVHとそれを用いた最適化の一例
当院における具体的な活用例
1.臨床で使用した治療計画との比較
当院でのRapidPlanの使用に当たり,最も症例数が多く,治療計画が画一的な前立腺がん症例を対象とした。最初に検討したことは,「実際に臨床使用してきた計画と比較して,RapidPlanを用いて作った計画がどうであるか」である。RapidPlanのモデルを作成した後,過去に治療を行った前立腺がんのVMAT計画10例を使って,RapidPlanを用いて再度最適化したものと比較した。当院で運用している2種類の計画標的体積(PTV:前立腺および前立腺+精囊近位)と直腸のDVHに着目して評価を行った。今回のRapidPlanのモデルには,過去の50症例を学習させた。最適化時は,RapidPlanにより計算された直腸のDVHの予測曲線を使って線量制約をかける方針とした。PTVの線量制約に関しては,PTVを線量分布のnormaliza-tionに用いるので固定値とした。
両方の計画のPTVの線量指標〔最大線量,最小線量,平均線量,homogeneity index(HI:最大線量/最小線量)〕を比較した結果,平均線量に0.2%程度の差が見られたが,最大・最小線量およびHIには差がなかった(図2)。一方,直腸のDVHに関しては,高線量側には差が認められなかったものの,低線量側においてRapidPlanで最適化した計画で線量が低い部分が見られた(図3)。これは,実際に臨床使用した計画では低線量側の線量制約がほぼなかったのに対し,RapidPlanではその部分にも制約条件がかかったので差が出たと考えられる。RapidPlanで作った計画の方が,PTVのカバレッジを保ちながらも全体的に直腸線量を下げることができたと言える。
当院の経験では,モデルに登録された症例が50例以上になると,計算回数も1回で満足できる線量分布を作成することができた。前立腺肥大が著明であったり,前立腺と直腸前壁が通常よりも広く接していたりするような症例でも,モデルに学習させる症例の種類を増やすことによって,試行錯誤することなく適正な線量分布を作成することが可能になると期待される。
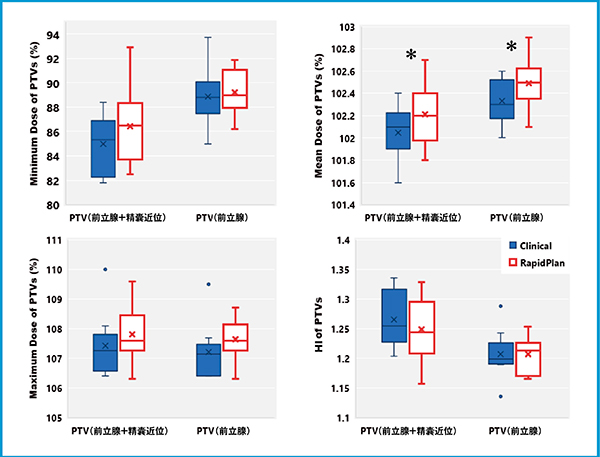
図2 臨床で使用した計画とRapidPlanの比較
PTVに対する各線量指標を比較した。Wilcoxonの符号順位検定では平均線量の比較において差(“*”, p0.05)が見られたが,ほかの指標に関しては有意な差とならなかった。
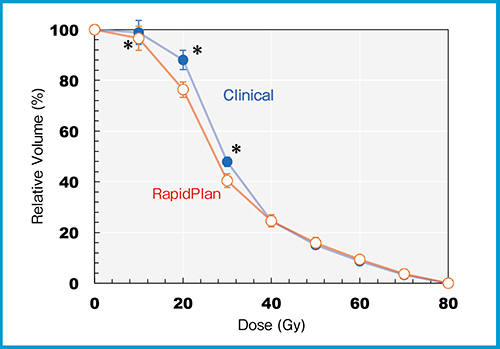
図3 直腸の平均DVH
エラーバーは1σ。「*」で示す値はWilcoxon符号順位検定でp0.01となったもの。
2.連携施設へのモデルの移行と共有
当院で前立腺がんVMATの治療計画にRapidPlanの臨床使用を開始してから,およそ半年後に当院の連携施設でVMATの立ち上げがあり,当院のモデルを活用することを試みた。当院で作成した学習データを匿名化したモデルをエクスポートし,連携施設のEclipseにインポートすることで,連携施設でも当院の学習データを使用することができるようになった。エクスポートおよびインポートにかかった時間はそれぞれ1分以内であった。VMATの経験がない施設でも,非常に良好な学習曲線で臨床導入することができた。また,連携施設で作成した計画と当院の学習データを基に作成した計画を直接比較することが容易であり,治療計画の品質管理の観点でもRapidPlanは有用だった。
まとめ
前立腺がん症例に対するRapidPlanの初期経験を報告した。テンプレートを用いた従来の治療計画と比較して,少なくとも同等ないし良好な線量分布が得られた。連携施設へのモデルの移行もスムーズに行えた。ハイボリュームセンターの経験を他施設でもすぐに導入することが可能であり,放射線治療の均てん化に寄与するツールであると考えられる。
