VARIAN RT REPORT
2022年11月号
人にやさしいがん医療を 放射線治療を中心に No.12
千葉県がんセンターにおける転移性脳腫瘍に対する定位放射線治療:HyperArcの臨床運用と活用
宮阪 遼平(千葉県がんセンター放射線治療部物理室)
はじめに
転移性脳腫瘍は,がん患者の8~10%に発症すると推定されており,患者の生活の質(QOL)と生存期間に影響を与えることが知られている1)。全脳照射は,歴史的に転移性脳腫瘍の標準治療として確立されてきたが,放射線照射による認知機能障害は無視できない有害事象として議論されている2)。定位放射線治療(stereotactic radiotherapy:SRT)は,病変に限局して高線量を投与する治療法であり,QOLの改善と正常脳の副作用の低減が期待される3)。従来のSRTはガンマナイフなどの専用機が用いられてきたが,コンピュータ性能の進歩により,近年では汎用リニアックを利用した照射技術も国際的に幅広く用いられている。“HyperArc”は,バリアン社が提供するSRTの治療オプションの一つである。本稿では,千葉県がんセンターにおけるHyperArcの運用方法とその活用について紹介する。
HyperArcとは
HyperArcは,頭蓋内腫瘍に対するSRTのワークフローを自動化するために開発された放射線治療計画装置「Eclipse」および放射線治療装置 「TrueBeam」(共にバリアン社製)のアプリケーションの総称である。HyperArcの機能は治療計画プロセスと患者治療プロセスで異なり,いずれもユーザーの業務負担を最小化する。
HyperArcの治療計画プロセスは,本質的に強度変調回転放射線治療(VMAT)と同じだが,腫瘍周囲への線量の広がりを最小限に抑えることを目的に,(1) 治療ビームの設定(アイソセンタ位置,コリメータ角度およびノンコプラナーアークの構成)を自動で決定する,(2) 専用の線量計算オプション“SRS-NTO(normal tissue objective) ”を用いて最適化計算する点で異なる。また,(3) 専用の患者固定具と組み合わせることでバーチャル・ドライランを実行し,患者と治療装置の干渉を未然に回避する。加えて,(4) 手作業によるパラメータ入力を省力化し,効率的な計画立案を可能にする。ここで,筆者が最も注目する機能は(1) 治療ビーム設定の自動化である。複数個の転移性脳腫瘍に対して単一アイソセンタの治療計画を立案する場合,2つ以上の腫瘍が同じマルチリーフコリメータ(MLC)ペアを共有することがある(図1 a)。この条件下では,腫瘍間の領域はMLC によって遮蔽されず,正常組織に照射される線量は増加する4)。HyperArcは,同じMLCペアを共有するターゲットの数が最小となるようにコリメータ角度を自動選択し(図1 b),不要な線量の広がりを低減する。
HyperArcの患者治療プロセスは,一連の照射を完全自動化することで治療時間の短縮を可能にする。また,あらかじめ設定された撮影スケジュール“Imaging WayPoints”に従い,ノンコプラナー照射前にmegavoltage(MV)X線画像を自動撮影し,必要に応じて患者位置を再修正する。一般に,転移性脳腫瘍の放射線治療では,治療時間が延長するほど治療中の患者移動は大きくなることが報告されている5)。より正確な患者固定が求められるSRTでは,わずかな患者移動であっても腫瘍に対する線量集中性を損なう危険性があることから,治療時間の短縮や治療中の画像照合は不可欠な要素と言えるだろう。
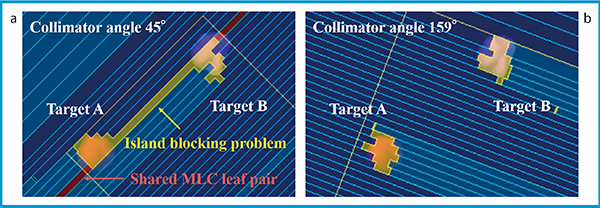
図1 複数のターゲットに対する単一アイソセンタ定位放射線治療のBeam’s eye view
MLCペアが複数のターゲットで共有される場合,ターゲット間の領域がMLC によって遮蔽されない問題“island blocking problem”が生じる(a)。HyperArcは,island blocking problemが起こりにくいコリメータ角度を自動選択し,不要な線量の広がりを低減する(b)。
HyperArcの臨床運用
千葉県がんセンターにおいて,HyperArcは単回,3分割および5分割のSRTに利用されている。直径10mm未満の微小な転移巣や5個以上の多数個の転移巣に関してもSRTの対象としており,HyperArc導入以降,延べ165件のSRTが実施された(2020年11月から2022年8月までの実績)。
HyperArcの治療計画は,腫瘍の数およびサイズによらず,腫瘍に対する高い線量集中性を示す(図2)。千葉県がんセンターにおいて,SRTの処方線量は,腫瘍径に応じて表1のとおり決定され,肉眼的腫瘍体積(GTV)に全方1mmのマージンを付与した計画標的体積(PTV)の95%以上に投与される(D95%処方)。加えて,50%等線量曲線は,SRS-NTOを用いて最適化計算することで,PTV表面から5mm以内に収まるように調整される。SRS-NTOのみでは低線量域の制御が困難となる場合,ターゲット周囲にリング状の輪郭を作成し,最適化計算に利用することで線量分布形状の改善を図る7)。HyperArcの導入以降,SRTの治療計画に要する時間は従来よりも短縮したため,患者治療はシミュレーションCT撮影から最短で2日後に開始される。
HyperArcの患者治療は,“semi-automation mode”と“full automation mode”に大別されるが,両者の違いは治療中の画像照合において患者位置を再修正できるか否かに限られる。そのため,Imaging WayPointsが設定されなければ照射モード間でリニアックの動作は変わらず,一連の照射は完全自動化される。千葉県がんセンターでは,semi-automation modeが採用され,高線領域とリスク臓器の位置関係や患者の全身状態に合わせて治療中の画像照合が適宜追加される。
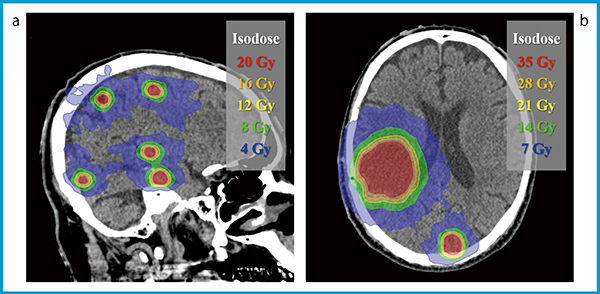
図2 HyperArcを用いて計画された定位放射線治療の線量分布
a:10個の微小な腫瘍に対する治療計画(20Gy/単回)
b:直径15mm(35Gy/5分割)および45mm(30Gy/5分割)の腫瘍に対する治療計画
表1 転移性脳腫瘍に対する定位放射線治療の処方線量
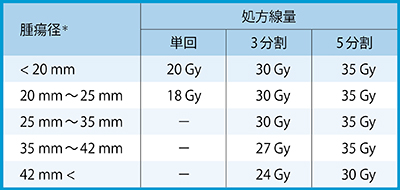
* 腫瘍径は等価直径で決定される。腫瘍と脳幹が重複する場合,腫瘍径によらず処方線量は25 Gy/5分割とし,脳幹の線量制約6)
(最大線量<31Gy,D1cc<26Gy)が優先される。
局所同時ブースト併用海馬抜き全脳照射への応用
千葉県がんセンターにおいて,HyperArcは局所同時ブースト併用海馬抜き全脳照射に応用されている8)。HyperArcは,海馬に対する線量低減(17Gy以下)と腫瘍に対する高線量投与(50Gy以上)を達成しながら,周囲の脳実質において高い線量均一性を示す(図3)。加えて,照射の完全自動化により治療時間を4分程度にまで短縮し,高いスループットを実現する。HyperArcは,頭蓋内腫瘍に対するピンポイント照射を目的に設計されたアプリケーションだが,計画者の工夫次第でより高度な治療計画に活用することも可能であり,臨床におけるさらなる活躍が期待される。
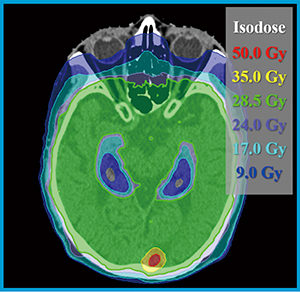
図3 HyperArcを用いて計画された局所同時ブースト併用海馬抜き全脳照射の線量分布
おわりに
本稿では,HyperArcの運用方法とその活用について臨床例を交えて紹介した。転移性脳腫瘍の治療方針は,腫瘍の数や大きさ,原発巣,患者の全身状態や治療歴などさまざまな情報を基に決定されるが,施設が所有する治療モダリティにも大きく左右される。つまり,SRTの実施が技術的に困難な場合,患者は全脳照射を選択するしかないのである。単発から小数個(2~4個)の転移性脳腫瘍に関しては,SRTの推奨グレードは高く,有効な治療効果が認められている9)。HyperArcは,技術的側面からわれわれユーザーを手助けし,臨床的側面から患者に有益な選択肢を提供するだろう。
●参考文献
1)Schouten, L.J., et al. : Incidence of brain metastases in a cohort of patients with carcinoma of the breast, colon, kidney, and lung and melanoma. Cancer, 94(10) : 2698-2705, 2002.
2)Gondi, V., et al. : Why avoid the hippocampus? A comprehensive review. Radiother. Oncol., 97(3) : 370-376, 2010.
3)Brown, P.D., et al. : Effect of Radiosurgery Alone vs Radiosurgery With Whole Brain Radiation Therapy on Cognitive Function in Patients With 1 to 3 Brain Metastases : A Randomized Clinical Trial. JAMA, 316(4) : 401-409, 2016.
4)Kang, J., et al. : A method for optimizing LINAC treatment geometry for volumetric modulated arc therapy of multiple brain metastases. Med. Phys., 37(8) : 4146-4154, 2010.
5)Mangesius, J., et al. : Intrafractional 6D head movement increases with time of mask fixation during stereotactic intracranial RT-sessions. Radiat. Oncol., 14(1) : 231, 2019.
6)Timmerman, R.D. : An overview of hypofractionation and introduction to this issue of seminars in radiation oncology. Semin. Radiat. Oncol., 18(4) : 215-222, 2008.
7)Clark, G.M., et al. : Plan quality and treatment planning technique for single isocenter cranial radiosurgery with volumetric modulated arc therapy. Pract. Radiat. Oncol., 2(4) : 306-313, 2012.
8)Hasegawa, Y. : A phase II trial of hippocampus sparing in whole-brain radiotherapy in patients with multiple brain tumors : Cognitive function and quality-of-life results. UMIN-CTR Clinical Trial, 2014.
https://center6.umin.ac.jp/cgi-open-bin/ctr_e/ctr_view.cgi?recptno=R000017359
9)脳腫瘍診療ガイドライン 2019年版 第2版. 日本脳腫瘍学会 編,日本脳神経外科学会 監修,金原出版,東京,2019.
https://www.jsn-o.com/guideline3/index1.html
